O vaskepulver det er et rengøringsmiddel, der er en del af dagligdagen for en stor del af befolkningen, da det bruges til at gøre det lettere at vaske folks tøj. Det er et produkt, der erstattede barsæbe, da folk i vaskeprocessen generelt havde for vane at gnide det på deres tøj.

Bar sæbe bruges stadig meget i f.eks. Opvask
Pulversæbe blev først fremstillet i 1946 efter nogle forsøg på at gøre brugen af barsæbe lettere. Et af forsøgene var at fremstille sæben i flager eller granulater. Disse forsøg var imidlertid ikke vellykkede, fordi sæben interagerer med ioner, der er til stede i hårdt vand, hvilket primært forringer rengøringshandlingen.
Hvorfor kan vi ikke kalde vaskemiddel på den måde?
Kemisk set kan vi ikke kalde vaskemiddel på den måde. Hvis vi ser på emballagen af disse produkter, vil vi se, at der står vaskemaskiner, ikke vaskepulver. Det er korrekt at kalde det Pulvervaskemiddel, da dets kemiske sammensætning er forskellig fra sammensætningen af en sæbe.
Kemien i vaskepulver, eller bedre, vaskepulver, er baseret på den grundlæggende forskel mellem en sæbe og et vaskemiddel. Se definitionen og de kemiske egenskaber ved disse materialer:
a) Vaskemidler:
De er kemiske stoffer, der har meget lange kæder (stor mængde kulhydrater) kun udgøres af kulstof- og brintatomer, der konfigurerer det, vi kalder regioner ikke-polær. I slutningen af denne lange kæde er der også en polær gruppe.
Den polære del af vaskemidlet skyldes tilstedeværelsen af en sulfonatgruppe, dvs. et svovlatom, der interagerer med tre iltatomer eller en fosfatgruppe, der har et fosforatom, der interagerer med tre atomer af ilt. Se repræsentationen af et vaskemiddels struktur:
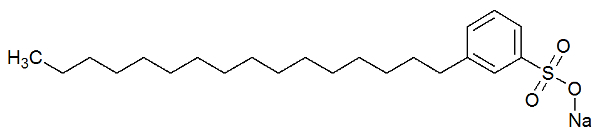
Strukturel formel for et vaskemiddel
Den polære del (dannet af natriumsulfonat) af vaskemidlet er i stand til at interagere med vandmolekyler. Den ikke-polære del (kun dannet af carbonatomer og hydrogener) interagerer med fedtmolekylerne. Således får vaskemidlet fedtet til at interagere med vandet og danne en emulsion.
b) Sæber
er salte af carboxylsyrer stammer fra den kemiske reaktion mellem fedtstoffer og stærke baser, såsom NaOH. Se repræsentationen af sæbens kemiske struktur:
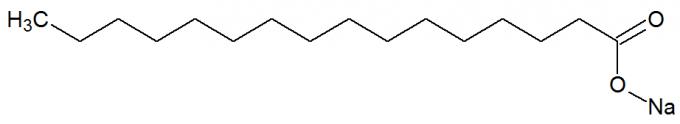
Strukturel formel af en sæbe
De har også lange kulstofkæder med en ikke-polær og polær del. På denne måde er sæbens ikke-polære del (kun sammensat af carbon og hydrogen) i stand til at interagere med fedtstoffer, og dets polære del (dannet af COONa-gruppen) med vand, danner emulsioner, såsom vaskemidler.
Som fokus for denne tekst er kemien af "sæbe" pulvereller rettere, den kemiske sammensætning af pulvervaskemidlet, vi præsenterer alle de kemiske stoffer, der er en del af dets sammensætning, såvel som vigtigheden af hver enkelt af dem:
Kemisk sammensætning af pulveropvaskemiddel
anionisk overfladeaktivt middel (såsom natriumalkylbenzensulfonat og natriumalkylethersulfonat). De binder sig til fedtmolekylet såvel som vandmolekylet og fjerner således fedtet fra vævet;
Enzymer: Lipaser og proteaser bruges til at fjerne pletter. Dette skyldes, at enzymer kemisk er biokemiske katalysatorer, der fremmer transformation af komplekse molekyler til enklere molekyler. Således kan mindre molekyler lettere fjernes fra tøj;
Blegemiddel (natriumperborat): Det virker ved oxidation, reduktion eller enzymatisk handling. I vand producerer det hydrogenperoxid, som er et stærkt oxidationsmiddel. De reagerer kemisk med beklædningsgenstandens pigment, ændrer strukturen og resulterer i en farveændring;
Optiske blokkere: de er stoffer, der absorberer ultraviolet stråling eller ultraviolet lys og kort derefter udsender et blåt fluorescerende lys, der f.eks. maskerer den gule farve på tøjet;
Dufte: De er essenser, der bruges til at efterlade en behagelig lugt på tøjet efter vaskeprocessen. Det er bemærkelsesværdigt, at dufte er essenser (de hører til esterfunktionen);
Farvestoffer: Stoffer, der bruges til at farve produktet
Sekvestrerings- og chelateringsmidler: EDTA (ethylendiamintetraeddikesyre) er et eksempel på en sekvestrerende middel. De interagerer med calcium-, magnesium- og jernioner, der hovedsagelig findes i hårdt vand, hvilket ikke tillader interaktion med nogen rengøringshandlingskomponent, såsom overfladeaktivt middel.
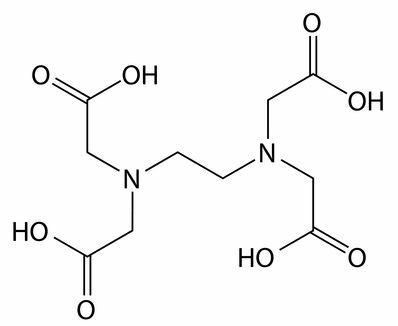
Strukturel formel for EDTA-sekvestranten
Af mig Diogo Lopes Dias
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/quimica-sabao-po.htm
