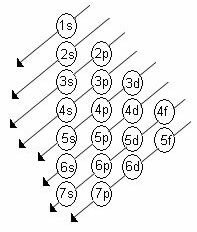
Alkalimetaller er kemiske grundstoffer, der findes i første gruppe med periodisk system, kaldet 1A-familien.
De får dette navn, fordi de let reagerer med vand og danner alkaliske stoffer såsom hydroxider.
De mest rigelige alkalimetaller på planeten er natrium (Na) og kalium (K).
Hvad er alkaliske metaller?
1A-familien er dannet af 6 metaller:
| Kemisk element | Atomnummer (Z) | Atommasse (u) | Elektronisk konfiguration |
|---|---|---|---|
| Lithium (Li) | 3 | 6,941 | 2s1 |
| Natrium (Na) | 11 | 22,9898 | 3s1 |
| Kalium (K) | 19 | 39,098 | 4s1 |
| Rubidium (Rb) | 37 | 85,47 | 5s1 |
| Cæsium (Cs) | 55 | 132,905 | 6s1 |
| Francio (Fr) | 87 | 223 | 7s1 |
Bemærk: Selvom brint (H) er placeret i 1A-familien, har det forskellige egenskaber end alkalimetaller og klassificeres som et ikke-metal.
De vigtigste egenskaber ved alkaliske metaller
- Har lav tæthed
- Ved stuetemperatur er de faste
- De er bløde og farvede metaller
- De er meget reaktive og gode ledere af elektricitet.
- De har lav elektronegativitet og ioniseringspotentiale
- Har høj elektropositivitet
- Reager let med vand og dann hydroxider
- Reager let med ilt og dann oxider
- Har kun 1 elektron i valensskallen
- Det har tendens til at miste denne elektron og danne monovalente kationer (med en +1 ladning)
- Den elektroniske konfiguration ender altid i ns1
Læs også: Periodiske bordfamilier
Alkaliske metalegenskaber
Kend de vigtigste egenskaber ved hvert alkalimetal:
- Lithium (Li): det hårdeste alkalimetal i familien med lav opløselighed og lavere densitet i denne gruppe. Det er en stor leder af elektricitet og meget reaktiv. Således reagerer det med vand og danner hydroxider og med luft og danner oxider.
- Natrium (Na): blødt metal, med lav densitet og moderat opløselighed. Det er en fremragende leder af elektricitet og meget reaktiv. Derfor reagerer det med vand og danner hydroxider og med luft og danner oxider.
- Kalium (K): blødt metal, med lav densitet og stærk leder af elektricitet. Det har god vandopløselighed og er meget reaktivt. Således reagerer det med vand og danner hydroxider og med luft og danner oxider.
- Rubidium (Rb): blødt metal med lav densitet og høj vandopløselighed. Det er en fremragende leder af elektricitet og meget reaktiv. Derfor reagerer det med vand og danner hydroxider og med luft og danner oxider.
- Cæsium (Cs): blødt metal med lav densitet og fremragende opløselighed i vand. Det er en fremragende leder af elektricitet og meget reaktiv. Dette element reagerer med vand og danner hydroxider og med luft og danner oxider.
- Francio (Fr): blødt metal, med lav densitet og fremragende vandopløselighed. Det er en stærk leder af elektricitet og meget reaktiv. Dette element reagerer med vand og danner hydroxider og med luft og danner oxider.
Læs også: Periodiske egenskaber
Alkaliske jordmetaller
Jordalkalimetaller repræsenterer de kemiske elementer i 2A-familien af periodiske system. De er faste, bløde og stoffer med lav densitet.
De får dette navn, fordi de oxider, de danner, blev kaldt jordarter.
Hvad er alkaliske jordmetaller?
2A-familien er dannet af 6 metaller:
| Kemisk element | Atomnummer (Z) | Atommasse (u) | Elektronisk konfiguration |
|---|---|---|---|
| Beryllium (Be) | 4 | 9,0122 | 2s2 |
| Magnesium (mg) | 12 | 24,312 | 3s2 |
| Calcium (Ca) | 20 | 40,08 | 4s2 |
| Strontium (hr.) | 38 | 87,62 | 5s2 |
| Barium (Ba) | 56 | 137,34 | 6s2 |
| Radio (Ra) | 88 | 226 | 7s2 |
Læs også:
- Lithium
- Barium
- Kemiske grundstoffer
- Elektronisk distribution
- Øvelser på det periodiske system