Som forklaret i teksten “Katalyse og katalysator”, Katalysatorer er kemiske arter, der fremskynder reaktionshastigheden. Dens anvendelse er meget nyttig i kemiske industrier, hvor det søges at spare så meget tid som muligt på produktionen.
I visse situationer er det imidlertid mere interessant, at reaktionen forløber langsommere; som for eksempel når du vil bestemme hastigheden af meget hurtige reaktioner. For at opnå denne bedrift, kontrollere og studere disse reaktioner, er det sædvanligt at tilføje et stof, der bremser reaktionerne, som kaldes hæmmere, gift eller antikatalysatorer.
Disse kemiske arter kombineres med katalysatoren, hvilket ophæver eller mindsker dens virkning. Dette er muligt, fordi katalysatorens virkningsmekanisme er at nedsætte aktiveringsenergien, lette reaktionsprocessen og øge dens hastighed; allerede inhibitorer virker omvendt, hvilket betyder at de øger den aktiveringsenergi, der er nødvendig for, at reaktanter kan nå det aktiverede kompleks.
Et eksempel, der kan nævnes, er arsen (As), som har denne funktion i Haber-Bosch-reaktionen, en reaktion, der er meget udbredt i industrien til produktion af ammoniak ved hjælp af jern (Fe
(s)) som katalysator. Således bliver jernens effektivitet meget lille i nærværelse af arsen, som hæmmer det, det vil sige det er katalysatorgiften ved denne reaktion, som er vist nedenfor: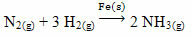
Arsen kan også udøve en antikatalytisk virkning, når der anvendes metallisk platin (Pt(s)) som en katalysator for SO-forbrændingsreaktionen2 (g), til produktion af svovltrioxid (SO3 (g)). Tilstedeværelsen af arsen, selv i små mængder, fjerner den katalytiske virkning af platin, som kan lamme en del af produktionen. Derfor anvendes normalt i industrier, der beskæftiger sig med denne produktion, divanadiumpentoxid (V2O5 (s)) som en katalysator i stedet for platin.
Stop ikke nu... Der er mere efter reklamen;)
Et andet eksempel forekommer i følgende hydrogenperoxid-nedbrydningsreaktion:
2 timer2O2 (aq) → 2 H2O(1) + 1 O2 (g)
I dette tilfælde er en hæmmer, der kan anvendes, noget syre, for når mediet er surt, forløber reaktionen langsommere.
Men hæmmeren bruges også i vid udstrækning af industrien, primært til at fungere som en reaktionshæmmer for den naturlige nedbrydning af fødevarer, drikkevarer, kosmetik og medicin.
Kosmetik kan f.eks. Tage lang tid at nå ud til forbrugeren; således anvendes forskellige konserveringsmidler i dem, såsom propylparaben, der anvendes i oliefasen og fungerer som en antisvamp, og methylparaben, der anvendes i den vandige fase, og som har en antiseptisk virkning. Deres respektive strukturer er vist nedenfor:
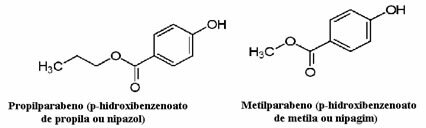
Det er interessant, at der på mange kosmetiske mærker er følgende sætning: “Det indeholder ikke parabener”. Dette betyder, at denne kosmetik ikke har disse konserveringsmidler, som vi nævnte, og at de normalt ikke er blevet testet på dyr.
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Katalysatorinhibitorer"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/inibidores-catalisador.htm. Adgang til 27. juni 2021.


