På kovalente bindinger, også kaldet molekylære eller homopolære bindinger, er dem, der forekommer mellem atomer af elektronegative elementer, det vil sige med en tendens til at modtage elektroner, etablere en binding af deling af elektroner fra deres valensskaller.
Kovalent binding kan forekomme mellem følgende elementer: brint, ikke-metaller og halvmetaller. Metaller deltager aldrig i denne type binding.
Lad os overveje et simpelt eksempel på en kovalent binding: den brintgasdannende binding (H2):
H + H → H2
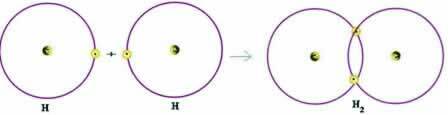
Bemærk, at begge atomer havde brug for at modtage en elektron for at fuldføre deres valensskal - ifølge Octet-reglen - og på denne måde at forblive stabil. Derfor delte de deres elektroner, og på denne måde havde de begge to elektroner, havde deres komplette K-skal og erhvervet konfiguration af ædelgashelium.
Denne deling af elektroner er det, der adskiller denne type binding fra ionbinding, hvor elektronoverførsel finder sted.
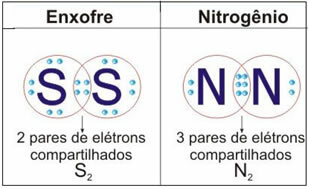
Se figuren nedenfor for yderligere to eksempler på denne sag:
Stop ikke nu... Der er mere efter reklamen;)
I denne type binding er der dannelsen af molekyler, som kan repræsenteres af deres respektive molekylære formler, det vil sige den enkleste repræsentation, der indikerer, hvor mange atomer af hvert element der er i molekylet. Nogle eksempler på molekylære formler er: H2, S2, O2nej2, H2O, CO2, etc.
Den kovalente binding kan repræsenteres af to andre formler:
- Elektronisk formel eller Lewis formel: i denne formel vises også elektronerne til hvert atoms valensskal og dannelsen af elektroniske par. Disse elektroner er symboliseret ved tegnene . eller x;
- Flad strukturformel eller kobberstrukturformel: viser elementernes links, hvor hvert delt par svarer til en bindestreg. Hvis det bare er et strejf, kalder vi det et enkelt link; hvis der er to, dobbeltbinding; og hvis der er tre bindestreger, tredobles det.
Se på andre eksempler på kovalente bindinger, der er repræsenteret ved disse tre kemiske formler:
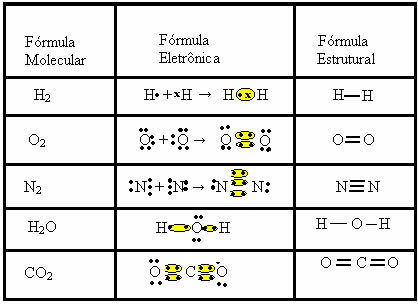
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Kovalente obligationer"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/ligacoes-covalentes.htm. Adgang til 27. juni 2021.