Den franske kemiker Joseph Louis Proust (1754-1826) fortsatte med at udføre omhyggelige eksperimenter, der relaterede masserne af komponenterne til visse reaktioner.
For eksempel er de grundstoffer, der udgør vand, brint og ilt. Proust fandt ud af, at hydrogen i denne vanddannende reaktion altid reagerede med ilt i et konstant og bestemt forhold, der var henholdsvis 1: 8. Se hvordan dette sker nedenfor:

Læg mærke til det uanset hvor meget masse af anvendte elementer, vil andelen altid være den samme.
Proust bemærkede, at dette ikke kun var tilfældet med vand, men med alle andre stoffer.
15,06 g kobbersulfid (CuS) dannes for eksempel ved omsætning af 10,00 g metallisk kobber (Cu) med 5,06 g svovl (S). Så hvis vi fordobler mængden af kobber (som går til 20,0 g), og hvis vi vil have alt kobberet til at reagere, det vil også være nødvendigt at fordoble svovlmængden til 10,12 g med den samlede dannelse på 30,12 g sulfid.
Hvis der nu tilføjes et beløb, der ikke er i forhold, vil det overskydende beløb blive tilovers, det vil ikke reagere. Bemærk dette nedenfor:
Stop ikke nu... Der er mere efter reklamen;)
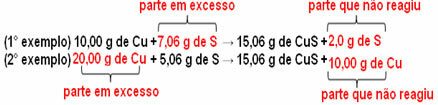
Læg mærke til det reaktionen finder kun sted i henhold til det definerede forhold. Derfor konkluderede Proust i 1799, at når flere stoffer kombineres for at danne en forbindelse, gøres dette altid i et defineret masseforhold.
Så han skabte en lov, der kaldes Prousts lov, Loven om konstante forhold eller Lov om definerede forhold, som er angivet som følger:

Denne lov og Lavoisiers lov (Lov om massebevarelse) er navngivet Vægtlove, fordi de taler i masser af involverede stoffer.
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Prousts lov eller lov om konstante forhold"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/lei-proust-ou-lei-das-proporcoes-constantes.htm. Adgang til 27. juni 2021.