Overvej den generiske reversible reaktion nedenfor, hvor små bogstaver svarer til de afbalancerede reaktionskoefficienter, og de store bogstaver er reaktanterne, og produkterne er alle luftformige:

I betragtning af hver af reaktionsretningerne separat, er deres udviklingshastigheder (Td) givet ved:
* Direkte reaktion: aA + bB → cC + dD
Alledirekte = Kdirekte. [DET]Det. [B]B
* Omvendt reaktion: cC + dD → aA + bB
Alleomvendt = Kbaglæns. [Ç]ç. [D]d
Den kemiske ligevægtskonstant med hensyn til koncentration i mængden af stof (Kç) og med hensyn til partialtryk (KP) gives ved at dividere Kdirekte af Kbaglæns.
Så vi har:
Kdirekte. [DET]Det. [B]B = 1 → Kdirekte__ = __[Ç]ç. [D]d___
Kbaglæns. [Ç]ç. [D]d Kbaglæns [DET]Det. [B]B
At være, Kç =_Kdirekte_
Kbaglæns
Så vi har:
Kç =__[Ç]ç. [D]d___ eller KP =__(Praça)ç. (pD)d___ |
Hvor p er partialtrykket for hvert stof ved ligevægt.
På denne måde hæves hver koncentration til en eksponent svarende til koefficienten for det respektive stof i reaktionen, og Kç har ikke enhed *.
Derudover er et meget vigtigt aspekt, der skal fremhæves, det i dette udtrykhverken faste komponenter eller rene væsker skal være repræsenteret., da kun ting, der kan lide variation, deltager i dette udtryk. Koncentrationen i stofmængden af et stof i fast tilstand er konstant og er således allerede inkluderet i værdien af K selv.ç. Det samme gælder for rene væsker som vand. Kort sagt, kun stoffer i gasformig tilstand og i vandig opløsning deltager i ekspressionen.
Stop ikke nu... Der er mere efter reklamen;)
Bemærk eksemplerne nedenfor:
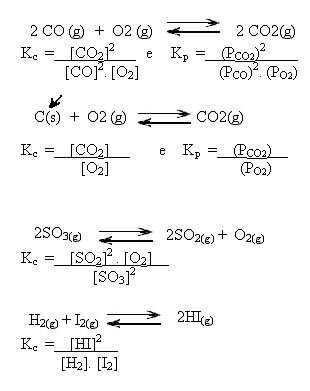
K-værdierç kan vise os, om koncentrationen af reaktanter og produkter er den samme, eller om den ene er større end den anden:
- hvis Kç eller KP er lig med en (Kç = 1)betyder dette, at koncentrationen af reaktanter og produkter er ens;
- hvis værdien af Kç eller KP være høj, betyder det, at produkterne er i større koncentration, fordi i udtrykket af Kç produkterne er i tælleren;
- hvis værdien af Kç eller KP er lavbetyder dette, at reagenserne er i højere koncentration, fordi i ekspressionen af Kç reagenserne er i nævneren.
* Kç og KP de er dimensionsløse tal, det vil sige rene tal, uden nogen enhed relateret til nogen størrelse eller relation mellem størrelser.
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Ligevægtskonstanter Kc og Kp"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm. Adgang til 28. juni 2021.