O ammoniumnitrat er et fast stof med molekylformel NH4VED3 og hvidt udseende (når det er rent). konstitueret ved ioner NH4+ (ammonium) og NO3- (nitrat), er ikke brandfarlig, men er stærkt oxiderende og reaktiv. Dens nedbrydningsreaktion genererer et stort volumen af gasser som produktet, hvilket gør upassende opbevaring af dette produkt til et alvorligt problem, da eksplosioner kan forekomme. Og også almindeligt anvendt i landbruget som gødning.
Læs også: Naturlige stoffer - molekyler stammer fra naturen
Hvad er ammoniumnitrat?

Ammoniumnitrat det er et salt konstitueret af NH-ioner4+ (ammonium) og NO3- (nitrat). Det er en fast forbindelse, der når det er rent, den er hvid i farven. Det er meget brugt som en landbrugsgødning, men det kan også bruges til fremstilling af sprængstoffer, som det er et meget oxiderende stofderefter oxiderende. Den løbende reaktion af ammoniumnitrat genererer en høj frigivelse af gasser, forårsager eksplosiv påvirkning.
Kendetegn ved ammoniumnitrat
Mol masse: 80,04336 g / mol.
Salt sammensat af ionerne: ammonium (NH4+) og nitrat (NO3-).
Udseende: hvidt fast stof.
Det er stærkt oxiderende.
Reagerer let med andre stoffer.
Det er ikke brandfarligt.
Til normale temperatur- og trykforhold:
- massefylde: 1,73 g / cm3;
- kogepunkt: 210 ° C
- smeltepunkt: 169,6 ° C;
- opløselighedsgrad i vand: 216 g / 100 ml;
- pH: 5,5 (0,2 M).
Ammoniumnitratformel
Molekylformlen for denne forbindelse er NH4VED3.
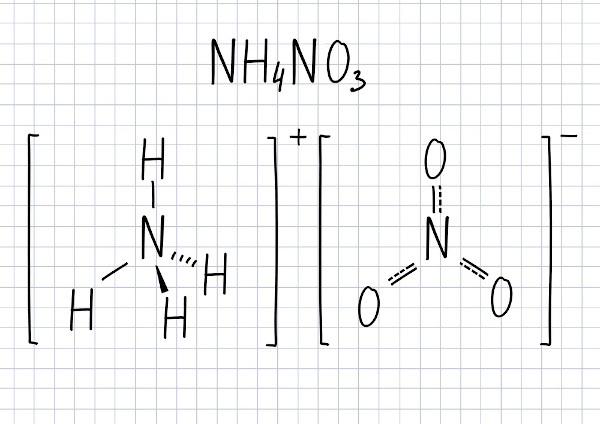
Nedbrydning af ammoniumnitrat
for at være en stof med høj reaktivitet og højt oxidationspotentiale ammoniumnitrat, når det udsættes for høj temperatur, udløser a nedbrydningsreaktion, og de vigtigste produkter er gasser, kvælstof, ilt og vanddamp. Nedbrydningen gives i to trin:
→ 1. trin:
2NH4VED3 (s) → 2N2O (g) + 4H2O (g)
→ 2. etape:
2N2O → 2N2(g) + O2(g)
→ Global ligning:
2NH4VED3 (s) → 2N2(g) + O2(g) + 4H2O (g)
Bemærk, at i den første ligninget af produkterne opnået i nedbrydningen er dinitrogenoxid (N2O), også kendt som lattergas. Det bruges til at øge kraften i bilmotorer til at forbrænde brændstof og som et bedøvelsesmiddel, hovedsageligt af tandlæger. Det er det også en af de vigtigste gasser, der er ansvarlige for drivhuseffekt.
Se også: Hvad er typerne af kemiske reaktioner?
Produktion af ammoniumnitrat
Ammoniumnitrat kan opnås ved reaktion mellem ammoniumsulfat (NH4)2KUN4 og calciumnitrat Ca (NO3)2. Se nedenunder:
(NH4)2KUN4 + Ca (NO3)2 → 2 NH4VED3+ Sag4
Det kan også fremstilles af gasformig ammoniak, der bobles i en salpetersyreopløsning, idet den har det vandige ammoniumnitrat som reaktionsprodukt. Se:
NH3 (g) + HNO3 (aq) → NH4VED3(her)
Anvendelse af ammoniumnitrat

- Gødningsproduktion
- Sprængstoffer i miner, stenbrud og byggeri
- Herbicider og insekticider
- Opnåelse af lattergas til industriel anvendelse
- Absorbenter til oxider
- Oxidant til raketdrivmidler
- Fremstilling af isotermiske poser
- Produktion af bedøvelsesrøg til behandling af nældefeber i biavl
Også adgang: Hvordan bekæmper man en brand?
Fare for ammoniumnitrat
En af de største risici forbundet med ammoniumnitrat er i utilstrækkelig opbevaring. Da det er et meget oxiderende stof, og det reagerer med flere andre forbindelser, udløser det a reaktion med frigivelse af et stort volumen gas. Forkert opbevaring er underlagt forurening med brandfarlige produkter, udsættelse for varme- eller gasretention, hvad der kan forårsage eksplosioner.
Dette er allerede sket i Texas i USA for eksempel med et fragtskib, der kom fra Frankrig med 2.086 tons ammoniumnitrat. ulykken skete i 1947 og blev kendt som Texas City Disaster. Tragedien forårsagede 581 menneskers død og det opstod på grund af en brand, der ikke var indeholdt i skibet, og som nåede ammoniumlasten, hvilket udløste eksplosionen.
Et andet eksempel var eksplosionssekvens der skete den 4. august 2020 i havnen i by Beirut, Libanon, efterlader mere end 100 mennesker døde og 5.000 sårede. Eksplosionsstørrelsen skyldtes antændelsen af en kædereaktion af lasten på 2.750 ton ammoniumnitrat, der var lagret der.
Det er også værd at bemærke, at ammoniumnitrat kan forårsage hud- og øjenirritation og ved indånding åndedrætsbesvær. I blodbanen har stoffet toksisk effekt, da det reagerer med kropsvæsker, og produkterne fra denne reaktion, såsom nitrat, kan forårsage sundhedsskader, såsom blå baby sygdom, også kendt som infantil methemoglobinæmi (lavt blodhæmoglobin). Denne sygdom er tilbagevendende i familier i landdistrikter på grund af forurening med ammoniumnitrat, der findes i gødning, af vandområder i landbrugsregionen.
af Laysa Bernardes
Kemilærer
Kilde: Brasilien skole - https://brasilescola.uol.com.br/quimica/nitrato-de-amonio.htm
