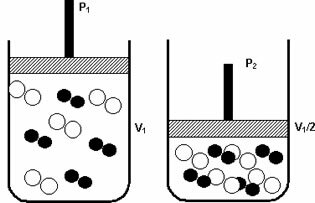
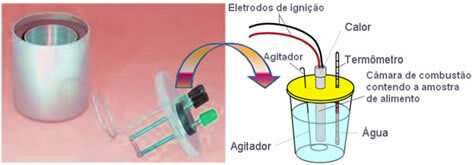
Reversible reaktioner starter normalt med en vis mængde reagenser. Når den direkte reaktion starter, forbruges disse reagenser over tid til dannelsen af produkterne, falder derfor koncentrationen af reagenserne, mens koncentrationen af produkterne øges. Derefter starter den omvendte reaktion også og producerer også reaktanterne, indtil udviklingshastigheden (hastigheden) for de direkte og inverse reaktioner forbliver den samme og når den såkaldte kemisk balance.
I ligevægt er der ligevægtskonstanten Kc, som grundlæggende udtrykkes ved:
|
Kc = [Produkter]koefficient i afbalanceret kemisk ligning [reagenser]koefficient i afbalanceret kemisk ligning |
Det vil sige i betragtning af følgende generiske ligevægtsreaktion:
a A + b B ↔ c C + d D
Da små bogstaver er koefficienterne, og de store bogstaver er stofferne, vil ligevægtskonstanten for denne reaktion være:
Kc = [Ç]ç. [D]d
[DET]Det. [B]B
Flere detaljer om dette kan ses i teksten Kc og Kp ligevægtskonstanter. Denne tekst viser os også noget vigtigt: at Kc-værdier kan vise os, om koncentrationen af reagenser og produkter er lige, eller hvis den ene er større end den anden, og som følge heraf, hvis den kemiske balance forskydes i en eller anden retning af reaktion.
Så vi er nødt til at bestemme værdien af Kc. For at gøre dette skal du huske, at disse beregninger er eksperimentelle, så lad os se på nogle eksempler på reaktioner og de data, der er opnået fra dem.
Noget, der er meget nyttigt ved udførelsen af disse beregninger, er at skrive en tabel svarende til den vist nedenfor og følge de trin, der er nævnt i den:

Tabel til at organisere de data, der bruges til at beregne ligevægtskonstanten
Lad os nu træne:
Eksempel 1: I en lukket beholder med en kapacitet på 2 liter ved en temperatur på 100 ° C er der 20 mol N2O4. Følgende reversible reaktion begynder at forekomme: N2O4 ↔ NEJ2. Efter nogen tid blev det fundet, at reaktionen nåede kemisk ligevægt, og at 8 mol NO2 havde dannet. Hvad er værdien af ligevægtskonstanten Kc ved en temperatur på 100 ° C?
Stop ikke nu... Der er mere efter reklamen;)
Løsning:
Lad os bruge tabellen:

Tabel anvendt til at løse ligevægtskonstantberegningseksempel
Bemærk, at i linjen, hvor mængderne, der reagerer og dannes, blev skrevet, ved vi, at der blev brugt 4 mol N2O4, fordi forholdet er 1: 2, og at der blev dannet 8 mol NO2.
Erstat nu bare de værdier, der findes i udtrykket af ligevægtskonstanten Kc i denne reaktion:
Kc = [VED2]2
[N2O4]
Kc = (4 mol / l) 2
(8 mol / l)
Kc = 2 mol / l
Værdien af Kc er dimensioneløs, den har ingen enhed relateret til nogen størrelse.
Lad os nu se på et eksempel, der også indeholder produkter fra begyndelsen:
Eksempel 2: I en lukket beholder med en kapacitet på 5 liter ved temperatur T er der 2 mol hydrogengas, 3 mol iodgas og 4 mol hydrogeniodid. Reaktionen går ind i kemisk ligevægt ved temperatur T, og det viser sig, at der er 1 mol brintgas i beholderen. Hvad er grafen, der repræsenterer denne ligevægt, og hvad er værdien af ligevægtskonstanten Kc ved temperaturen T?
Løsning:
Brug af tabel:
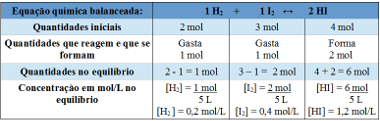
Tabel, der bruges til at bestemme ligevægtskonstanten
Grafen, der viser variationerne i mol / L-koncentrationer af reagenser og produkter, indtil de når ligevægt, kan gives ved:

Kemisk ligevægtsdiagram, der viser ændringer i koncentrationer af reagenser og produkter
Nu finder vi værdien af ligevægtskonstanten:
Kc = __ [HI]2__
[H2 ]. [JEG2]
Kc = (1,2)2
0,2. 0,4
Kc = 18
Af Jennifer Fogaça
Uddannet i kemi
Vil du henvise til denne tekst i et skole- eller akademisk arbejde? Se:
FOGAÇA, Jennifer Rocha Vargas. "Beregning af ligevægtskonstanten Kc"; Brasilien skole. Tilgængelig i: https://brasilescola.uol.com.br/quimica/calculo-constante-equilibrio-kc.htm. Adgang til 28. juni 2021.
Kemi

Test din viden og lær mere med denne liste over løste øvelser på kemiske balancer. Gennem dette materiale vil du være i stand til bedre at forstå, hvordan man arbejder med ligevægtskonstanter (Kp, Kc og Ki), ligevægtsforskydning, pH og pOH samt ligevægt i såkaldte bufferopløsninger.