Introduktion
Når et legeme modtager en vis mængde termisk energi, kan det variere dets temperatur eller dets fysiske tilstand, dvs. fast, flydende og gas. Temperaturvariationen opstår på grund af den øgede agitation af de partikler, der udgør kroppen, i dette tilfælde kaldes den mængde varme, som kroppen modtog fornuftig varme. Hvis kroppen ændrer sin fysiske tilstand ved konstant temperatur, siger vi, at mængden af varme kaldes latent varme. Men hvad er varme? Hvordan overføres det?
Varme er termisk energi i transit, hvilket bestemmes af temperaturforskellen mellem de involverede systemer. Varme strømmer fra legemet med højere temperatur til legeme med lavere temperatur og kan overføres fra et legeme til et andet på følgende måder: ledning, konvektion og bestråling. Udtrykket varme bruges til at indikere den overførte energi. Angivet med bogstavet Q er varmeenheden i det internationale system for enheder joule (J), opkaldt efter den engelske fysiker James Prescott Joule. Den mest anvendte enhed er imidlertid kalorien (cal), men vi kan relatere den til joule som følger:
Termisk kapacitet og specifik varme
Antag at der ikke er nogen ændring i fysisk tilstand, forestil dig en krop, der modtager en vis mængde energi og ændrer temperaturen. Det kaldes termisk kapacitet C, også kaldet varmekapacitet, kvotienten mellem mængden af varme (Q) og variationen i temperatur, som kroppen lider af (At), se:
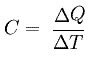
Enheden med termisk kapacitet er kalorien pr. Grad Celsius (cal / ° C).
Det er defineret som specifik varme, også kaldet termisk kapacitet, den numeriske værdi af den varmemængde, der forårsager variationen på en grad Celsius i et gram af stoffet. Matematisk definerer vi det som forholdet mellem varmekapaciteten og kroppens masse.

Den specifikke varmeenhed er cal / g ° C.
Grundlæggende ligning af kalorimetri
Ved at kombinere ligningerne, der definerer varmekapacitet og specifik varme, kan vi nå frem til ligningen der tilvejebringer mængden af fornuftig varme, der udveksles af kroppen med masse m, når dens temperatur ændres.
Q = m.c.AT
Hvor c er stoffets specifikke varme, og ΔT er stoffets temperaturvariation.
Af Marco Aurélio da Silva
Brazil School Team
Se mere!!
Kalorimeter og varmeveksling
Ved hvad et kalorimeter er beregnet til.
Termologi - Fysik - Brasilien skole
Kilde: Brasilien skole - https://brasilescola.uol.com.br/fisica/propagacao-calor.htm
