Spørgsmål om kemiske balancer i Enem er meget tilbagevendende. Med dette i tankerne skabte vi dette materiale, der bringer de vigtigste emner om denne gren af fysisk kemi, der er dækket af National High School Exam (Enem).
Blandt de spørgsmål, der er relateret til kemisk ligevægt, har vi ligevægtskonstant med hensyn til koncentration i mol / L og med hensyn til tryk, ionisk ligevægtskonstant, ioniseringskonstant, ligevægtsforskydning, pH og pOH, hydrolysekonstant, buffer og konstant af opløselighed.
Blandt de emner, der er beskrevet ovenfor, får nogle af dem større fremtrædende plads i Enem:
Balance skift
Ioniseringskonstant
pH
saltvandshydrolyse
Videolektion om kemisk balance på enem
1. Ligevægtsskift i Enem
1.1- (Enem 2015) Hypoxi eller højdesyge består af nedsat ilt (O2) i det arterielle blod i kroppen. Af denne grund oplever mange atleter ubehag (hovedpine, svimmelhed, åndenød), når de praktiserer fysisk aktivitet i store højder. Under disse betingelser vil der være et fald i koncentrationen af iltet hæmoglobin (HbO2) i balance i blodet ifølge forholdet:
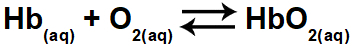
Ændringen i koncentrationen af iltet hæmoglobin i blodet opstår på grund af:
a) forhøjelse af blodtrykket.
b) stigningen i kropstemperatur.
c) reducere temperaturen i miljøet.
d) faldet i iltpartialtryk.
e) faldet i mængden af røde blodlegemer.
Oxygeneret hæmoglobin (HbO2) findes i reaktanterne (højre side) af ligningen. Øvelsen spørger, hvilke af mulighederne der vil føre til en ændring i iltet hæmoglobin i blodet, det vil sige, det vil flytte balancen til venstre eller til højre.
a) Falsk. Øget blodgennemstrømning har intet at gøre med øget blodtryk.
b) Falsk. Temperaturen ændrer ikke den leverede balance.
c) Falsk. Temperaturen ændrer ikke den leverede balance.
d) Sandt. At reducere det delvise iltryk reducerer mængden af iltet hæmoglobin og skubber balancen til venstre.
e) Falsk. Faldet i antallet af røde blodlegemer vil medføre, at både antallet af hæmoglobiner og iltede hæmoglobiner falder.
1.2- (Enem 2011) Sodavand er blevet flere og flere mål for folkesundhedspolitikker. Limprodukter indeholder fosforsyre, et stof, der er skadeligt for fiksering af calcium, et mineral, der er hovedkomponenten i tandmatrixen. Karies er en dynamisk proces med ubalance i processen med dental demineralisering, tab af mineraler på grund af surhed. Det er kendt, at hovedkomponenten i tandemaljen er et salt kaldet hydroxyapatit. Sodavand, ved tilstedeværelse af saccharose, sænker pH-værdien af biofilmen (bakteriel plak), hvilket forårsager demineralisering af tandemaljen. Spytforsvarsmekanismer tager 20 minutter til 30 minutter at normalisere pH-niveauet og remineralisere tanden. Følgende kemiske ligning repræsenterer denne proces:

I betragtning af at en person indtager læskedrikke dagligt, kan der forekomme en proces med dental demineralisering som et resultat af den øgede koncentration af:
a) OH-, som reagerer med Ca-ioner2+, skubber balance til højre.
b) H+, som reagerer med OH-hydroxylerne-, skubber balance til højre.
c) OH-, som reagerer med Ca-ioner2+, skubber balance til venstre.
d) H+, som reagerer med OH-hydroxylerne-, skubber balance til venstre.
e) Ca2+, som reagerer med OH-hydroxylerne-, skubber balance til venstre.
Ret svar: Bogstav B
Løsning
Demineraliseringsprocessen skifter balancen til højre. Når personen drikker sodavand, indtager de et surt materiale, dvs. øger mængden af H+ i midten. H+ interagerer hurtigt med OH- af ligevægt, hvilket reducerer mængden af OH-. På denne måde flyttes balancen til højre og demineraliserer tanden.
1.3- (Enem-2013) Et af trinene i vandbehandling er desinfektion, hvor kloring er den mest anvendte metode. Denne metode består i at opløse klorgas i en opløsning under tryk og anvende den på det vand, der skal desinficeres. De involverede kemiske reaktionsligninger er:

Desinfektionsvirkningen styres af hypochlorsyre, som har et desinfektionspotentiale, der er ca. 80 gange større end hypochloritanionen. Mediets pH er vigtig, fordi det påvirker, i hvilket omfang hypochlorsyre ioniserer. For at desinfektionen skal være mere effektiv, skal pH i vandet, der skal behandles, være tættere på:
a) 0
b) 5
c) 7
d) 9
e) 14
Ret svar: Bogstav B
Ifølge teksten udføres stoffet HClO den bedste desinfektionsmiddelhandling. Derfor skal enhver fortolkning og konklusion rettes mod en måde at opnå dette stof på.
Stoffet HClO er til stede i den anden balance, så en interessant taktik er at flytte denne balance til venstre. I henhold til princippet om Le Chatelier, har vi muligheden for at øge mængden af H+ (tilsætning af et surt stof, pH mindre end 7) eller øg mængden af Cl-.
Det er bemærkelsesværdigt, at der i den første ligning er en anden kemisk ligevægt, der præsenterer HClO-arten-, som har tilknytning til H+, skubber balance til venstre. Dette er et skridt, vi ikke ønsker.
Derfor skal vi bruge en sur pH (under 7). Imidlertid bør denne pH ikke være for sur til at undgå mange H-kationer.+ i midten.
Se også:Kemisk balance i huler
2. pH og saltvandshydrolyse i Enem
2.1- (Enem-2017) Flere naturlige produkter kan fås fra planter gennem ekstraktionsprocessen. Lapachol er af naphthoquinon-klassen. Dens struktur har en enolhydroxyl (pKa = 6,0), der gør det muligt at isolere denne forbindelse fra ip-savsmuld ved ekstraktion med en passende opløsning efterfulgt af simpel filtrering. Overvej, at pKa = -log Ka, og at Ka er syrekonstanten i lapacholioniseringsreaktionen.

Hvilken løsning skal bruges til at ekstrahere lapachol fra ipê savsmuld mere effektivt?
a) Na-opløsning2CO3 til dannelse af et lapacholsalt.
b) Eddikesyre / natriumacetatbufferopløsning (pH = 4,5).
c) NaCl-opløsning for at øge ionstyrken af mediet.
d) Na-opløsning2KUN4 til dannelse af et ionpar med lapachol.
e) HCI-opløsning for at ekstrahere den ved hjælp af en syre-base-reaktion.
Erklæringen indikerer, at stoffets pKa er 6,0. Denne pKa-værdi skal bruges i pKa-udtrykket:
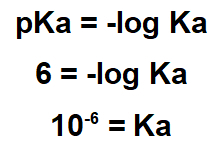
Da din Ka er lille, er lapachol et surt stof, så det er nyttigt at bruge et basisk stof for at fjerne det.
a) Sandt. Salt er grundlæggende, da det kommer fra en stærk base (fordi det er fra IA-familien) og CO3 kommer fra en svag syre (H2CO3).
b) Falsk. Pufferopløsningen er sur, og vi har brug for en base.
c) Falsk. NaCl er et neutralt salt, da det kommer fra en stærk base (fordi det er fra IA-familien), og Cl kommer fra en stærk syre (HCI).
d) Falsk. På2KUN4 er et neutralt salt, da Na kommer fra en stærk base (fordi det er fra IA-familien) og SO4 kommer fra en stærk syre (H2KUN4).
det er falsk. HCI er en syre, og vi har brug for en base.
2.2- (Enem- 2014) Med det formål at minimere miljøpåvirkninger bestemmer brasiliansk lovgivning, at kemiske rester, der frigives direkte i det modtagende organ, har en pH-værdi mellem 5,0 og 9,0. Et vandigt flydende affald genereret ved en industriel proces har en hydroxylionkoncentration lig med 1.0.10-10 mol / l. For at overholde lovgivningen adskilte en kemiker følgende stoffer, der er tilgængelige i virksomhedens lager: CH3COOH, Na2SO4, CH3OH, K2CO3 og NH4Cl.
Stop ikke nu... Der er mere efter reklamen;)
Hvilket stof kunne bruges til at justere pH-værdien, for at remanensen kunne frigives direkte i det modtagende legeme?
a) CH3COOH
b) I2KUN4
c) CH3Åh
d) K2CO3
e) NH4Cl
Ret svar: Bogstav D
Løsning
Trin 1: Bestem restkoncentrationens pH.
Øvelsen indikerer, at remanensen har en hydroxidkoncentration, der er lig med 10-10.
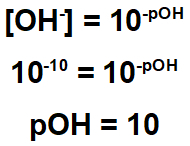
Derfor kan vi beregne pH af denne rest:

Fra ovenstående har vi, at remanensen har en sur karakter, da dens pH er mindre end 7. For at neutralisere det er det således vigtigt at bruge et stof med en grundlæggende karakter.
Trin 2: Bestem karakteren af hvert salt for at angive, hvilken der er basisk, som CH3COOH (alternativ a) er en syre, og CH3OH (alternativ c) er en alkohol, organisk klasse med sur karakter.
b) Neutralt salt, da Na kommer fra en stærk base (fordi den er fra IA-familien), og SO4 kommer fra en stærk syre (H2KUN4).
d) Basissalt, da K kommer fra en stærk base (fordi det er fra IA-familien) og CO3 kommer fra en svag syre (H2CO3).
e) Syresalt som NH4 kommer fra en svag base (NH4OH), og Cl kommer fra en stærk syre (HCl).
2.3- (Enem- 2014) En forsker bemærker, at etiketten på et af krukkerne, hvor han opbevarer et koncentrat af fordøjelsesenzymer, er ulæselig. Han ved ikke, hvilket enzym glasset indeholder, men har mistanke om, at det er en gastrisk protease, der fungerer i maven ved at fordøje protein. Ved at vide, at fordøjelsen i maven er sur og tarmen er basisk, samler han fem reagensglas med mad forskelligt, tilsæt enzymkoncentratet til opløsninger med en bestemt pH og vent på at se, om enzymet virker i nogen deres. Testrøret, hvor enzymet skal virke for at indikere, at forskerens hypotese er korrekt, er det, der indeholder:
a) kartoffelterning i opløsning med pH = 9.
b) stykke kød i opløsning med pH = 5.
c) kogt æggehvide i opløsning med pH = 9.
d) del af nudler i opløsning med pH = 5.
e) smørkugle i opløsning med pH = 9.
Ret svar: Bogstav B
Øvelsen kræver af den studerende god fortolkning og sammenhæng med biokemisk viden om fødevarer. Han oplyser, at forskeren mener, at enzymet er fordøjelsessystemet, virker ved en sur pH og virker på proteiner (fordi det er en protease).
Hvis dette enzym virker i et surt miljø, skal pH være mindre end 7. Kød består af proteiner, mens pasta består af kulhydrater. Så det rigtige svar er alternativ b.
2.4- (Enem- 2012) En husmor tabte ved et uheld vand fra afrimningen af en fisk i køleskabet, hvilket efterlod en stærk og ubehagelig lugt inde i apparatet. Det er kendt, at fiskens karakteristiske lugt skyldes aminer, og at disse forbindelser opfører sig som baser. I tabellen er brintkoncentrationerne af nogle materialer, der findes i køkkenet, angivet, som husmor overvejer at bruge, når hun rengør køleskabet.

Blandt de anførte materialer, hvilke er passende til at lindre denne lugt?
a) Alkohol eller sæbe
b) Citronsaft eller alkohol
c) Citronsaft eller eddike
d) Citronsaft, mælk eller sæbe
e) Sæbe eller sodavand
Ret svar: Bogstav C
Løsning
Øvelsen foreslår en problematisk situation, hvor en husmødres køleskab har en stærk lugt forårsaget af et stof af grundlæggende karakter. Således stilles det spørgsmålstegn ved, hvilke materialer der ville være interessante at løse dette problem.
For at neutralisere en base er det nødvendigt at bruge et surt materiale eller med en pH lavere end 7. Hvordan motion gav værdierne for H-koncentrationer+ af materialerne var det nok at bruge hver enkelt i nedenstående udtryk:

Dermed:
Saft: pH = 2
Mælk: pH = 6
Eddike: pH = 3
Alkohol: pH = 8
Sæbe: pH = 12
Tønde: pH = 12
Materialer med en sur karakter er juice, eddike og mælk. Således er det kun alternativ c, der bringer materialer af sur karakter.
3. Ligevægtskonstant i Enem
3.1- (Enem-2016) Efter fuldstændig slitage kan dækkene brændes til elproduktion. Blandt de gasser, der genereres ved fuldstændig forbrænding af vulkaniseret gummi, er nogle forurenende stoffer og forårsager sur regn. For at forhindre dem i at flygte ud i atmosfæren kan disse gasser bobles ind i en vandig opløsning indeholdende et passende stof. Overvej stofoplysningerne anført i nedenstående tabel:

Blandt de stoffer, der er anført i tabellen, er den, der er i stand til effektivt at fjerne forurenende gasser (a)
a) phenol.
b) pyridin.
c) methylamin.
d) kaliumhydrogenphosphat.
e) kaliumhydrogensulfat.
Ret svar: Bogstav D
Løsning
Øvelsen udgør en problematisk situation, hvor forurenende gasser fremmer sur regn. Derefter spørger han, hvilke af de nævnte stoffer, der ville være interessante at neutralisere disse gasser og følgelig undgå sur regn.
For at undgå sur regn skal syregasser neutraliseres ved hjælp af en basisk opløsning. Stoffer med denne egenskab er dem, der fortrinsvis frigiver OH-grupper- i midten. I tabellen er pyridin, methylamin og kaliumhydrogenphosphat basiske stoffer.
For at bestemme det stof, der er i stand til at fjerne forurenende gasser mere effektivt, skal vi analysere værdien af ioniseringskonstanten. Jo større konstanten er, jo større er evnen til at frigøre OH-. Så kaliumhydrogenphosphat det er det mest egnede stof i dette tilfælde.
3.2- (Enem-2015) Flere syrer anvendes i industrier, der bortskaffer deres spildevand i vandområder, såsom floder og søer, hvilket kan påvirke miljøbalancen. For at neutralisere surheden kan calciumcarbonatsalt tilsættes spildevandet i passende mængder, da det producerer bicarbonat, som neutraliserer vandet. Ligningerne involveret i processen præsenteres:

Baseret på værdierne af ligevægtskonstanterne for reaktionerne II, III og IV ved 25O C, hvad er den numeriske værdi af ligevægtskonstanten for reaktion I?
a) 4,5x10-26
b) 5x10-5
c) 0,8x10-9
d) 0,2 x 105
e) 2,2 x 1026
Ret svar: Bogstav B
Løsning
Denne øvelse involverer konstant ionisering. Oprindeligt er det vigtigt at forstå, at ligning I faktisk er resultatet (summen) af ligning II, III og IV. Derfor skal vi bruge principperne for at starte beslutningen Hess's lov.
Trin 1: Brug af Hess 'lov.
Når vi vender ligning II og holder ligninger III og IV, har vi:
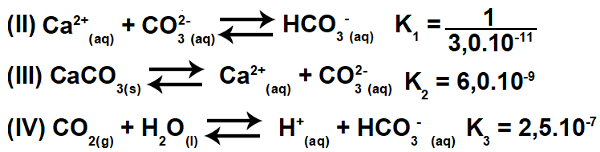
Således kan vi observere, at anionen CO3-2 og H-kationen+ vil blive elimineret, og summen af ligningerne vil resultere i ligning I.
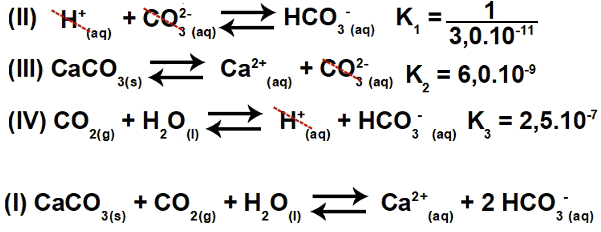
Trin 2: konstant beregning
Ligevægtskonstanten for ioniseringsligningen gives altid ved at multiplicere konstanterne for de andre ligninger:

Af mig. Diogo Dias