Teorie hybridizace se ukázala jako doplněk k Teorie oktetu, dokázat vysvětlit strukturu většího počtu molekul, včetně molekul vytvořených bórem (B).
Tento prvek má pět základních elektronů s následující elektronickou konfigurací:
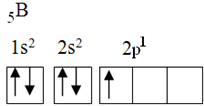
Podle teorie oktetu mohl bór vytvořit pouze jednu kovalentní vazbu, protože má pouze jednu neúplnou atomovou oběžnou dráhu. Experimentálně je však třeba poznamenat, že tento prvek tvoří sloučeniny, ve kterých provádí více než jednu vazbu.
Příkladem je fluorid boritý (BF3). Jak je uvedeno níže, bór vytváří tři kovalentní vazby s fluorem a sdílí tři páry elektrony a mající šest elektronů ve své poslední skořápce (valenční vrstvě), tj. výjimka z pravidla oktet.
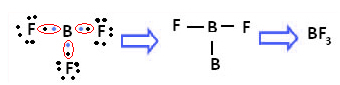
To je vysvětleno hybridizačním jevem, ke kterému dochází u boru. Ukázalo se, že elektron z podúrovně 2s absorbuje energii a přejde do vzrušeného stavu, ve kterém skočí do prázdné oběžné dráhy podúrovně 2p. Tímto způsobem se vytvoří tři neúplné orbitaly, které nyní mohou vytvořit tři kovalentní vazby:
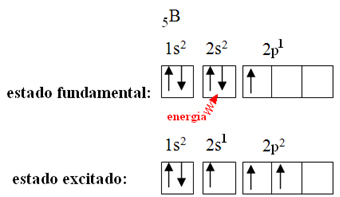
Vazby vytvořené v fluoridu boritém jsou však všechny stejné, ale pokud se podíváme výše, existují dvě vazby odlišné, protože jeden z nich by byl vyroben pomocí orbitálu a další dva pomocí orbitálu tohoto typu. typ p. To je místo, kde probíhá hybridizace, to znamená, že neúplné orbitaly se slučují a vedou ke třem
hybridní orbitaly nebo hybridizováno, které jsou identické a odlišné od originálů:Nepřestávejte... Po reklamě je toho víc;)
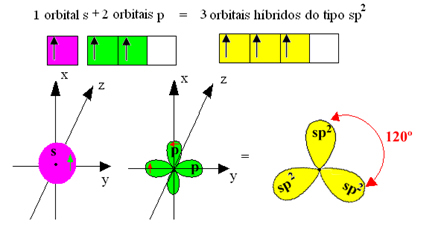
Jelikož se tyto hybridní orbitaly skládají z jednoho orbitálu a dvou p orbitalů, nazývá se tato hybridizace sp² hybridizace.
Fluor, který se váže na bór, má devět elektronů. Jeho elektronická distribuce a orbitaly jsou uvedeny níže:
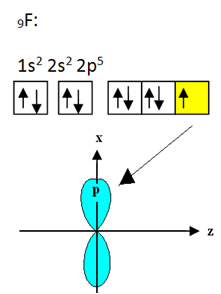
Všimněte si, že každý atom fluoru může vytvořit pouze jednu kovalentní vazbu a že orbitál, který tuto vazbu vytváří, je typu p. Níže tedy pozorujte, jak se utvářejí orbitaly při vytváření spojení, která tvoří BF3 a podívejte se, jak jsou odkazy identické σp-sp2:
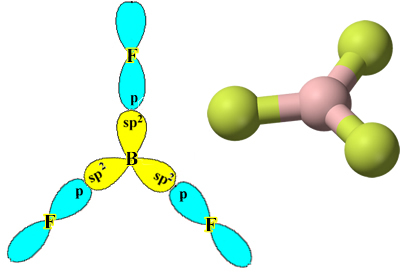
To se děje také u jiných prvků, viz například text „Hybridizace berylia”.
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Hybridizace boru“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/hibridizacao-boro.htm. Zpřístupněno 28. června 2021.