Na běžné baterie se nazývají Leclanché baterie pojmenovaný po svém vynálezci, francouzském chemikovi George Leclanché (1839-1882).

George Leclanché (1839-1882)
Leclanché vytvořil tento typ baterie v roce 1866. Také se jí říká suchá buňka protože do té doby existovaly pouze baterie, které používaly vodné roztoky, jako např Daniellina hromada.
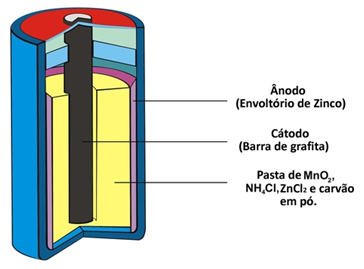
Dvě další jména, která tento typ hromady obdrží kvůli své konstituci, jsou kyselina hromada nebo zinko-uhlíková baterie. V zásadě je tvořen povlakem zinku odděleného od ostatních chemických látek, které tvoří hromádku, pomocí porézního papíru.
Tento zinek odpovídá zápornému pólu článku nebo anody, protože oxiduje a ztrácí dva elektrony podle níže uvedené semi-reakce:
Záporný pól - anoda: Zn (s) → Zn2+(tady) + 2 a-
Tato hromada má také kladný pól, katodu, což je grafitová tyč instalovaná uprostřed hromady obklopená oxidem manganičitým (MnO2), práškové uhlí (C) a vlhká pasta obsahující chlorid amonný (NH4Cl), chlorid zinečnatý (ZnCl2) a voda (H2Ó).
Chlorid amonný a chlorid zinečnatý jsou soli kyselého charakteru, odtud název „kyselá buňka“.
Grafitová tyč vede elektrony ztracené zinkem k manganu a redukuje oxid manganičitý (MnO)2) na oxid manganatý (Mn2Ó3), podle následující poloreakce:
Kladný pól - katoda: 2 MnO2 (aq) + 2 NH41+(tady) + 2e- → 1 Mn2Ó3(s) + 2NH3 (g) + 1 hodina2Ó(1)
Nepřestávejte... Po reklamě je toho víc;)
Vlhká pasta působí jako solný bod a umožňuje migraci hydroxylových aniontů (OH-) od grafitu po zinek.
Celková reakce je dána:
Zn (s) + 2 MnO2 (aq) + 2 NH41+(tady) → Zn2+(tady) + 1 mil2Ó3(s) + 2NH3 (g)
Tyto baterie proto nejsou dobíjecí, protože veškerý oxid manganičitý se přeměňuje na oxid manganičitý. Když baterie přestane fungovat, musí být zlikvidována.
DDD těchto baterií je 1,5V. Amoniak (NH3 (g)) vytvořené na katodě lze uložit na grafitovou tyč, čímž brání průchodu elektronů a snižuje napětí baterie. Chcete-li se vrátit do normálního provozu, nechte baterii odpočívat mimo zařízení, protože zinkový kation (Zn2+(tady)) vytvořený na anodě reaguje s amoniakem a ponechává grafitovou tyč volnou.
Kromě toho může také pomoci umístění hromady do chladničky, protože snížení teploty zvýhodňuje rozpustnost amoniaku ve vlhké pastě v hromádce.
Dalším důležitým faktorem suchých buněk Leclanché, který musíme vzít v úvahu, je to zinkové pouzdro může korodovat, a tím unikat korozivní materiál a poškodit zařízení.. Nejlepší proto je nenechávat baterie uvnitř zařízení, která nejsou používána nepřetržitě.
Suché baterie jsou určeny pro zařízení, která vyžadují lehké a trvalé vybití, jako jsou dálkové ovládání, nástěnné hodiny, přenosné rádio a hračky.
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Suchý stoh Leclanché“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/pilha-seca-leclanche.htm. Zpřístupněno 28. června 2021.
