Vy estery jsou okysličené organické sloučeniny, které vznikají chemickou reakcí mezi a karboxylová kyselina to je alkohol. Představte funkční skupinu (složenou ze dvou atomů kyslíku a dvou radikály R) znázorněno níže:
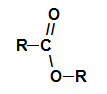
Obecná funkční skupina esteru
Strukturálně, co charakterizuje ester je to přítomnost nějakého alkylového radikálu připojeného přímo k atomu kyslíku. V tomto případě radikál (R) navázaný na uhlík - který je zase dvojnásobně navázán na kyslík - může být buď alkylový radikál nebo atom vodíku.
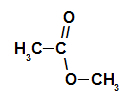
Uhlíkový řetězec esteru
esterifikační reakce
jde o chemická reakce, při které vznikne ester a molekula vody z interakce mezi karboxylovou kyselinou a jakýmkoli alkoholem, jako v níže uvedené rovnici:
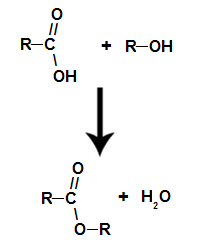
Chemická rovnice představující vznik esteru
Během esterifikace interaguje hydroxylová skupina (OH) alkoholu s vodík (H) ionizovatelný z hydroxylové skupiny kyseliny a tvoří molekula vody.
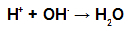
Molekula vody tvořící skupiny při esterifikaci
již ester vzniká spojením radikálu (R) alkoholu s kyslíkem, který po tvorbě vody zůstane z hydroxylové skupiny kyseliny.
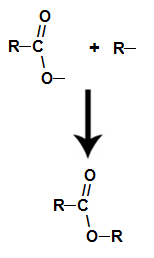
Tvorba molekuly esteru
Vlastnosti esterů
Hlavní fyzikální vlastnosti prezentované estery:
Mají ovocné a květinové aroma;
nízké estery molární hmotnost jsou kapalné při pokojové teplotě a ty s vysokou molární hmotností jsou pevné;
Ve srovnání s alkoholy a karboxylovými kyselinami mají estery nižší teploty tání a teploty varu;
Ve srovnání s vodou jsou estery s nižší molární hmotností méně husté;
Estery s nižší molární hmotností jsou polární a ty s vyšší molární hmotností nepolární;
V polárních esterech převládají síly permanentní dipól; v nepolárních silách převládají indukovaný dipól;
Estery s nižší molární hmotností jsou špatně rozpustné ve vodě a estery s větší hmotností jsou nerozpustné ve vodě.
Jedno pravidlo pojmenování Ester
Před použitím pravidla pojmenování a esterJe třeba si uvědomit, že tato sloučenina je tvořena spojením dvou částí, z nichž jedna pochází karboxylové kyseliny (červeně) a druhé alkoholu (modře), jak je znázorněno na obrázku a následovat:
Nepřestávejte... Po reklamě je toho víc;)
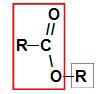
Identifikace částí, z nichž pochází ester
Podle Mezinárodní unie pro čistou a aplikovanou chemii (IUPAC), oficiální pravidlo pro pojmenování esteru je:
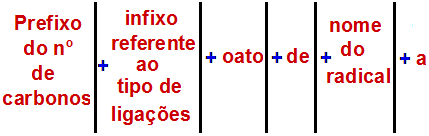
Jedno pravidlo pojmenování Ester
Poznámka: Předpona a infix vždy odpovídají části karboxylové kyseliny a radikál odpovídá části alkoholu.
Níže uvádíme několik příkladů použití pravidla pojmenování pro estery:
1. příklad: malinová esence
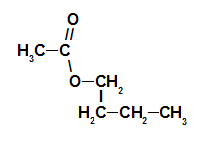
Strukturní vzorec esteru malinové esence
K pojmenování tohoto esteru používáme:
Předpona čÓ uhlíků: et, protože tvořící se kyselina má dva uhlíky;
Infix o typu odkazů: an, protože tvořící se kyselina má pouze jednoduché vazby mezi uhlíky;
akt;
v;
Radikální: butylza to, že má čtyři uhlíky v pořadí;
The.
Název esteru odpovídající malinové esenci je tedy butyl ethanoát.
2. příklad: esence šišky
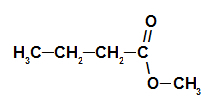
Strukturní vzorec esteru borové šišky
K vytvoření názvu tohoto esteru používáme:
Předpona čÓ uhlíků: ale, protože tvorba kyseliny má čtyři uhlíky;
Infix o typu odkazů: an, protože tvořící se kyselina má pouze jednoduché vazby mezi uhlíky;
akt;
v;
Radikální: methyl, protože tvořící se alkohol má pouze jeden uhlík;
The.
Název esteru odpovídající esencii borovicového kužele je tedy methyl butanoát.
3. příklad: jahodová esence
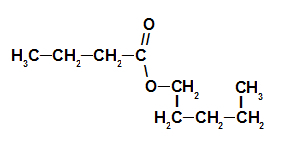
Strukturní vzorec esteru jahodové esence
K pojmenování tohoto esteru používáme:
Předpona čÓ uhlíků: ale, protože tvořící se kyselina má čtyři uhlíky;
Infix o typu odkazů: an, protože tvořící se kyselina má pouze jednoduché vazby mezi uhlíky;
akt;
v;
Radikální: pentyl, protože tvořící se alkohol má pět uhlíků za sebou;
The.
Název esteru odpovídající jahodové esenci je tedy pentylbutanoát.
Použití esterů
Estery jsou dobře známé pro své použití jako příchuť ve zpracovaných potravinách, tj. látkách, které simulují charakteristickou chuť a aroma přírodních potravin, jako je ovoce. Dále estery se stále používají při výrobě léků, kosmetiky, parfémů a vosků.
Podle mě. Diogo Lopes Dias
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
DNY, Diogo Lopes. „Co je to ester?“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ester.htm. Zpřístupněno 28. června 2021.
Chemie

Estery, příchutě potravin, příchutě, esterifikační reakce, methylantranilát, pentyl-acetát, butyl-etanoát, ethyl-butanoát, propanetriol, glycerin, stearin.