Podle prvního zákona termodynamiky v každém termodynamickém procesu množství tepla Q přijatý systémem se rovná jeho práci plus variaci jeho vnitřní energie.
Když je tlak konstantní, teplo vyměněné systémem s externím médiem se používá k práci a ke změně vnitřní energie. V mnoha praktických situacích jsou systémy vystaveny atmosférickému tlaku, jako v případě chemické reakce. Obrázek výše ukazuje FV diagram tohoto typu procesu.
V tomto případě, v rovnici prvního zákona,
Q = τ + ∆U
žádný z výrazů není nula. Práce je psána jako funkce objemové variace volumeV, jako například:
τ = P.∆V
Pro konkrétní případ ideálního monoatomového plynu lze energii napsat takto:

Proto můžeme napsat první zákon termodynamiky jako funkci ΔV:


Teplo vyměněné s médiem je (5/2) P.ΔV a 40% z celkového množství - což odpovídá P.ΔV - se používá k provádění práce; a (3/2) P.ΔV, což odpovídá 60% z celkového počtu, se používají ke změně vnitřní energie. Tento výsledek platí pro ideální jednoatomový plyn.
Teplo souvisí s kolísáním teploty (podle zákona o ideálním plynu):
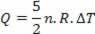
Dodané teplo lze tedy vypočítat změnou teploty nebo změnou objemu.
Autor: Domitiano Marques
Vystudoval fyziku
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/fisica/primeira-lei-para-processos-isobaricos.htm
