geometrický izomer je druh vesmírná izomerie který hodnotí a porovnává polohu v prostoru ligandů dvou atomů uhlíku v řetězci. Toto hodnocení je provedeno z imaginární roviny mezi zúčastněnými uhlíky.
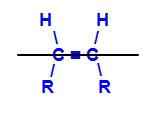
Imaginární rovina dělící molekulu
Pomyslná rovina ve struktuře nahoře rozděluje molekulu na horní rovinu a spodní rovinu. Díky tomu můžeme vyhodnotit a porovnat uhlíkové ligandy zapojené do každé z těchto rovin. Podívejte se na typy geometrických izomerů:
→ Cis-trans geometrický izomer
Sloučenina má cis-trans geometrická izomerie když řetězec zobrazí:
Otevřený řetězec s dvojnou vazbou mezi dvěma uhlíky, které mají navzájem stejné spojky. Viz příklad:
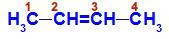
Strukturní vzorec but-2-enu
Ve struktuře můžeme pozorovat, že jak uhlík 2, tak uhlík 3 mají stejné ligandy, kterými jsou vodík (H) a methyl (CH3).
Uzavřený řetězec se dvěma uhlíky, které mají navzájem stejné ligandy. Viz příklad:
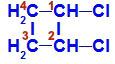
Strukturní vzorec 1,2-dichlorcyklobutanu
Ve struktuře můžeme pozorovat, že jak uhlík 1, tak uhlík 2 mají stejné ligandy, kterými jsou vodík (H) a chlor (Cl).
K vysvětlení izomerismu cis-trans použijeme but-2-en:
a) Cis izomer: je geometrický izomer, ve kterém stejné ligandy zaujímají stejnou rovinu. V níže uvedeném příkladu jsou vodíky na stejné rovině, stejně jako methylové radikály.

Strukturní vzorec cis-but-2-enu
b) Trans izomer: je geometrický izomer, ve kterém různé ligandy zaujímají stejnou rovinu. V níže uvedeném příkladu máme na stejné rovině vodík a methyl (CH3).
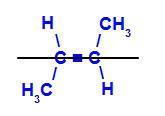
Strukturní vzorec trans-but-2-enu
Nepřestávejte... Po reklamě je toho víc;)
→ Geometrický izomer E-Z
Sloučenina má geometrický izomerismus E-Z, když řetězec má:
Otevřený řetězec s dvojnou vazbou mezi dvěma uhlíky, které mají všechny nebo některé odlišné linkery. Viz příklad:
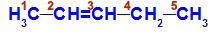
Strukturní vzorec pent-2-en
Ve struktuře vidíme, že uhlík 2 má methylový ligand (CH3) a vodík (H) a uhlík 3 obsahuje vodík (H) a ethyl (H) ligand3C-CH2).
Uzavřený řetězec se dvěma uhlíky, které mají všechny nebo některé ligandy navzájem odlišné. Viz příklad:
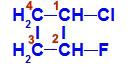
Strukturní vzorec l-chlor-2-fluor-cyklobutanu
Ve struktuře můžeme pozorovat, že uhlík 1 má jako hlavní ligandy vodík a chlor a uhlík 2 má jako hlavní ligandy vodík a fluor.
POZNÁMKA: Z různých ligandů v geometrické izomerii hodnotíme složitost ligandu (počet atomů) nebo atomové číslo.
Pro vysvětlení izomeru E-Z použijeme jak pent-2-en, tak 1-chlor-2-fluor-cyklobutan:
a) E-izomer
geometrický izomer kde složitější ligandy nebo ty s nejvyšším atomovým číslem jsou umístěny na opačných rovinách. V následujícím příkladu je nejsložitější ligand na uhlíku 2 methyl a nejsložitější ligand na uhlíku 3 je ethyl, které jsou umístěny v různých rovinách.
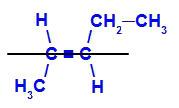
Strukturní vzorec E-pent-2-enu
b) Izomer Z
geometrický izomer kde složitější ligandy nebo ty s nejvyšším atomovým číslem jsou umístěny ve stejné rovině. V následujícím příkladu je ligandem s největším atomovým číslem uhlíku 1 chlor (Z = 17) a ligandem s největším atomovým číslem uhlíku 2 je fluor (Z = 9), které jsou umístěny ve stejné rovině.
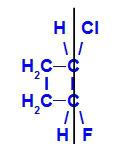
Strukturní vzorec Z-l-chlor-2-fluor-cyklobutanu
Podle mě. Diogo Lopes Dias
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
DNY, Diogo Lopes. „Co je to geometrický izomerismus?“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria-geometrica.htm. Zpřístupněno 28. června 2021.
Chemie
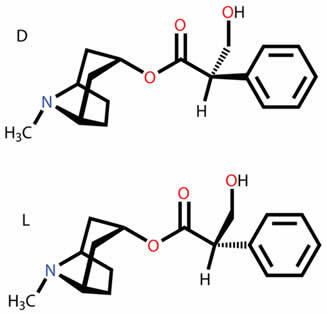
Zjistěte, o čem jsou různé typy rovinných a prostorových izomerů, jako je funkce, poloha, řetězec, tautomerismus, metamerismus, cis-trans geometrický a optický izomerismus.