Od starověku se člověk zajímal o zodpovězení otázky o složení hmoty.
Několik osobností z vědecké komunity se k tomuto tématu postavilo, ale až na konci 19. století se záhady o atomovém složení začaly odhalovat.
Například starověký filozof Leucippus věřil, že atom je tvořen malými částicemi.
Po této definici navrhli Democritus a Dalton, že atomové částice jsou masivní a nedělitelné.
Tato skutečnost byla později zpochybněna Thomsonem, anglickým fyzikem, který objevil existenci elektronu a byl schopen potvrdit myšlenku dříve navrženou Leucipem.
Po tomto objevu Thomson představil model, ve kterém byl atom tvořen sférou kladných nábojů a uvnitř jádra byly elektrony.
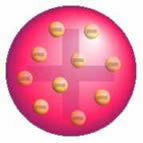
Thomsonův model atomu - v kladně nabité, rovnoměrně rozložené hmotové sféře,
byly by pokryty záporně nabitými elektrony, jako v pudinku.
I po Thomsonově teorii měl atomový model stále teoreticko-experimentální nedostatek, schopný prokázat svou pravdivost.
O tomto tématu se opět vřele diskutovalo, když tým fyzika Rutherforda zaznamenal, že došlo k velmi velké odchylce (a podle teorie pudinkové rozinky nevysvětlitelné), když některé radioaktivní alfa částice prošly tenkou vrstvou laminy kovový.
Po analýze a prostudování skutečnosti dospěl Rutherford k závěru, že poloměr atomu je 10 000krát větší než poloměr jádra.
Během celého studia atomu dospěl Rutherford a jeho tým v roce 1911 k atomovému modelu, kterému říkali planetární model atomu.

V roce 1913 rozluštil Niels Bohr atomový model a na své studie použil kvantum akce objevené Planckem. Kvantum akce bylo ve skutečnosti velkou zástupnou kartou, která měla dokončit a objasnit atomový model.
Bohr efektivně a jednoduše upravil model představený Rutherfordem a dospěl k následujícímu závěru:
Elektron získává energii, která je reprezentována definovanou dráhou. Povolené dráhy tvoří energetické úrovně.

Autor: Talita A. andělé
Vystudoval fyziku
Tým brazilské školy
Fyzika Moderní - Fyzika - Brazilská škola
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/fisica/do-atomo-rutherford-ao-atomo-bohr.htm
