THE ozonová vrstva, jak název napovídá, je vrstva nebo povlak tvořený molekulami ozonového plynu (O3 (g)), alotropní forma kyslíku, jejíž molekula je uvedena níže:
Nachází se ve vrstvě mimo atmosféru, v nadmořské výšce mezi 20 a 35 km, která se nazývá stratosféra. Ale tento plyn lze také najít v menším množství v troposféře (nadmořská výška asi 10 km).

Ozonová vrstva hraje zásadní roli při udržování života na Zemi, as je schopen absorbovat až 99% ultrafialové (UV) záření ze Slunce. Vzhledem k tomu, že toto záření má krátké vlnové délky a vysokou energii, má vysokou schopnost pronikání kůží. Je to toto záření, které způsobuje opalování, ale je také zodpovědné za mnoho škodlivých účinků, protože může poškodit DNA (deoxyribonukleová kyselina) a způsobit genetické mutace.
UV záření se dělí na tři odlišné energetické rozsahy: UVA (320 nm až 400 nm), UVB (290 nm až 320 nm) a UVC (200 nm až 290 nm). Mezi nimi je nejškodlivější a nejenergetičtější UVC, které naštěstí nedosahuje zemského povrchu, protože je filtrováno vrstvou. ozonu.
Ozónová vrstva je tedy opravdu všestranný a účinný štít, který pomáhá chránit před tímto škodlivým zářením. mnoho forem života, jako je plankton, které jsou zodpovědné za produkci velké části našeho kyslík.
Množství ozonu ve stratosféře není konstantní, ale je přímo úměrné intenzitě UV záření. K tvorbě molekul tohoto plynu dochází rozkladem molekul kyslíku (O2 (g)), tvořící volný kyslík, který ve druhém kroku reaguje s plynným kyslíkem:
1. krok:2 (g) → 2 O.(G)
2. etapa: The(G) + O.2 (g) → 13 (g)
V ozonové vrstvě se poté vytvoří chemická rovnováha:
2 O.2 (g) ↔ 1 O.3 (g) + O.(G) ∆H = + 142,35 kJ / mol
Bohužel však v průběhu času lidé uvolňovali některé znečišťující sloučeniny, které tuto rovnováhu posunuly směrem k rozkladu ozón, což snižuje jeho koncentraci ve stratosféře a nechává planetu nechráněnou.
Jednou z největších příčin zničení vrstvy Ozonem jsou CFC (chlorfluoruhlovodíky, také známé jako Fréons®), což jsou sloučeniny tvořené atomy uhlíku, fluorem a chlorem. CFC se uvolňují do atmosféry především díky jejich použití jako hnací plyn ve formě aerosolu (spreje), v ledničkách a ledničkách, jako expanzní prostředek na plasty a v rozpouštědlech k čištění elektronických obvodů.

Jak můžete vidět z níže uvedených reakcí, když CFC zasáhne stratosféru, sluneční záření rozkládá jeho molekuly a uvolňuje chlór. Chlor zase reaguje s ozonem a to snižuje jeho koncentraci:
CH3Cℓ(G) → CH3(G)+Cℓ(G)
Cℓ(G) + O.3 (g) → C.ℓÓ(G) + O.2 (g)
Kromě toho CℓVytvořený také reaguje s volnými atomy kyslíku v atmosféře a uvolňuje více atomů chloru, které budou reagovat s ozonem a stále více ničí naši ochrannou vrstvu:
ClO(G) + O.(G) → Cl(G) + O.2 (g)
Nejhůře postiženým místem je Antarktida, kde byla díra v ozonové vrstvě dvakrát větší než v Evropě v září 2000. Družice pro sledování ozonu NASA zaznamenala největší díra, jakou kdy v Antarktidě viděli, měří asi 28,3 milionu kilometrů čtverečních, což představuje více než trojnásobek rozlohy Austrálie. Tato situace je v Antarktidě horší, protože tam je tvorba atomů chloru velmi velká a zůstává nezměněna kvůli atypickému Stratosférické mraky se vytvořily během australské zimy a reakce se vyskytují na povrchu částic těchto mraků zobrazeno.
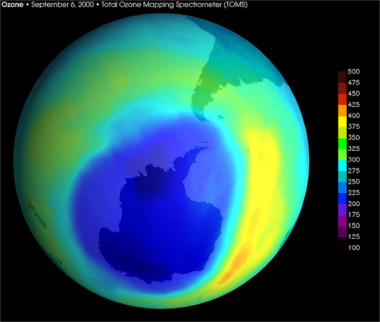
Satelitní snímek NASA „díry“ v ozonové vrstvě nad Antarktidou, září 2000
Možné důsledky destrukce ozonové vrstvy jsou:zvýšení výskytu rakoviny kůže v důsledku působení ultrafialových paprsků a zesílení globálního oteplování, což vede k různým katastrofickým výsledkům, jako je tání polárních ledovců, zvyšování hladiny vody v oceány.
Ale od roku 2000 stále existuje záblesk naděje koncentrace vCFCs klesly o téměř jedno procento ročně.
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/camada-de-ozonio2.htm