Studenti středních škol jsou vždy vystaveni čelení redoxní reakce s ionty, a to jak na přijímacích zkouškách, tak na zkoušce National High School Exam (Enem). Vyvažování těchto rovnic může být tedy velmi obávaným předmětem.
V zájmu snazšího porozumění tomuto tématu se tento text snaží oslovit vyvážení redoxních rovnic s ionty s popisem některých kroků k jeho provedení. Za tímto účelem musíme začít identifikováním tohoto typu chemické reakce.
Na redoxní reakce s ionty jsou identifikovány přítomností jedné nebo více složek s náboji (kladnými nebo zápornými), tj ionty (kationty nebo anionty), které mohou být přítomny v činidlech nebo produktech, jako ve dvou příkladech a následovat:
1. příklad:Cr2Ó72- + Fe2+ + H+ → Cr3+ + Fe3+ + H2Ó
2. příklad:Cl2 + C + H2O → CO2 + H+ + Cl-
Provést vyvažování rovnic redoxních reakcí s ionty, je nezbytné dodržovat některé kroky, například:
1. krok: určit NOX každého z atomů reaktantů a produktů rovnice;
2. krok: zkontrolujte, který druh utrpěl oxidace;
3. krok: Určete variaci NOX druhy, které prošly oxidací;
4. krok: vynásobte variaci nalezenou ve třetím kroku počtem atomů oxidujících druhů;
5. krok: zkontrolujte, který druh utrpěl snížení;
6. krok: Určete variaci NOX u druhů, které podstoupily redukci;
7. krok: vynásobte variaci nalezenou ve třetím kroku počtem atomů druhu, který redukuje;
8. krok: použijte hodnotu nalezenou ve čtvrtém kroku jako koeficient druhu, který se snižuje;
9. krok: použijte hodnotu zjištěnou v sedmém kroku jako koeficient oxidujících druhů;
10. krok: Uveďte koeficienty u ostatních druhů podle metody zkušební vyvážení. U druhů, kde to není možné, vložte neznámé jako koeficienty;
11. krok: vynásobte koeficient každého druhu jeho zátěží;
12. krok: Vyrovnejte součet nábojů reaktantů s množstvím produktů, abyste našli koeficient jednoho z neznámých druhů;
13. krok: Dokončení zůstatku pomocí zkušební metody.
Pro usnadnění porozumění postupujte podle výše popsaných kroků, v následujícím příkladu a redoxní rovnice s ionty:

Iontová rovnice ukazující některé ionty a obecné skupiny náboje 0
1. krok: NOX každého atomu.

NOX atomů přítomných v rovnici
2. krok: Druhy, které podléhají oxidaci.

Druhy, které podléhají oxidaci v rovnici
Vzhledem k tomu, že se NOX jódu zvyšuje z -1 na 0 z reaktantu na produkt, dochází k oxidaci právě u tohoto druhu.
3. krok: Určete variaci NOX oxidovaných druhů.
Chcete-li to provést, odečtěte nejvyšší NOX od nejnižší NOX:
∆NOX = (0) – (-1)
∆ NOX = 0 + 1
∆ NOX = 1
Krok 4: Násobení NOX množstvím.
V tomto kroku vynásobíme variaci nalezenou ve třetím kroku počtem atomů druhu.
Já- = ∆NOX.1
Já- = 1.1
Já- = 1
5. krok: Druhy, které podléhají redukci.

Druhy, které trpí snížením rovnice
Jelikož NOX chromu klesá z +7 na +3 z reaktantu na produkt, redukce proto prochází druh.
6. krok: Určete variaci NOX u redukovaných druhů.
Chcete-li to provést, odečtěte nejvyšší NOX od nejnižší NOX:
∆NOX = (+6) – (+3)
∆ NOX = +6 – 3
∆ NOX = 3
7. krok: Násobení NOX množstvím.
V tomto kroku vynásobíme variaci nalezenou v šestém kroku počtem atomů druhu.
Cr2Ó72- = ∆NOX.1
Cr2Ó72- = 3.2
Cr2Ó72- = 6
8. krok: Začněte vyvažovat.
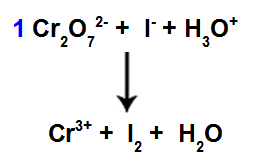
Začátek vyvažování pomocí nalezeného koeficientu
V tomto kroku zahájíme vyvážení umístěním koeficientu nalezeného ve čtvrtém kroku u druhů, které utrpěly redukci.
9. krok: Pokračujte ve vyrovnávání.

Pokračování vyvážení pomocí nalezeného koeficientu
10. krok: Použijte zkušební metodu.
V reaktantu je 6 atomů I, takže musíme dát I koeficient 32 produktu, protože jsou v něm pouze 2 atomy Cl;
Stejně jako u druhů 1, Cr2Ó72-, existují 2 atomy Cr, měli bychom dát koeficient 2 do druhu Cr3+ produktu.
Jelikož máme kyslík u tří druhů a u dvou z nich neexistují žádné koeficienty, abychom pokračovali v rovnováze, musíme do zbývajících druhů umístit neznámé:
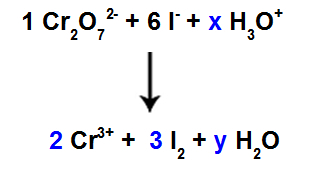
Koeficienty po použití zkušební metody
11. krok: Násobení každého druhu podle jeho zatížení.
Chcete-li to provést, jednoduše vynásobte koeficient druhu jeho zatížením, a to následujícím způsobem:
V činidlech:
Cr2Ó72- = 1.(-2) = -2
Já- = 6.(-1) = -6
H3Ó+ = x. (+ 1) = + x
Na produktech:
Cr3+ = 2.(+3) = +6
Já2 = 4.0 = 0
H2O = y.0 = 0
12. krok: Součet poplatků.
V tomto kroku musíme přidat množství reagencií a produktů nalezených v kroku 11:
Činidla = produkty
-2 + (-8) + (+ x) = +6 + 0 + 0
-2 - 6 + x = 6
-8 + x = 6
x = 6 + 8
x = 14
13. krok: Konec vyvážení.
K dokončení vyvážení musíme:
Výsledek nalezený ve 12. kroku u druhu H3Ó+;
Protože nyní máme v činidle 42 atomů H, je nutné umístit koeficient 21 do druhu H2V produktu.
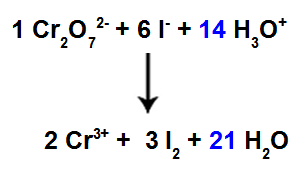
Rovnice vyvážené iontové reakce
Podle mě. Diogo Lopes Dias
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao-com-ions.htm

