Stejně jako cyklány, alkeny, alkyny, mimo jiné alkadienes také trpět hovory adiční reakce. V textu o reakce u dienůzjistíte, že adiční reakce závisí na typu dienu, na kterém se pracuje. Dienes lze obecně rozdělit na:
kondenzované nebo akumulované (žádná jednoduchá vazba mezi těmito dvěma zdvojnásobí);
Příklad: H2C = CH-CH3
konjugované nebo alternované (pouze jednoduchá vazba mezi těmito dvěma zdvojnásobí);
Příklad: H2C = CH — CH = CH2
izolovaný (alespoň dvě jednoduché vazby mezi těmito dvěma zdvojnásobí).
Příklad: H2C = CH-CH2—CH2—CH = CH2
Diels-Alderova reakce byl vyvinut v roce 1928 dvěma německými chemiky, Otto Paul Hermann Diels a Kurt Alder. Jedná se o velmi důležitou reakci v rámci organické chemie, protože umožňuje:
identifikovat dienové uhlovodíky;
získat nasycené cyklické uhlovodíky (výhodně cyklohexany).
K této organické reakci dochází pouze v alkadienů nebo konjugovaných nebo střídaných dienů a je volán doplněk 1.4. Sloučeninou, ve které můžeme jednodušeji pozorovat přidání 1,4, je but-1,3-dien, zobrazený níže:
H2C = CH — CH = CH2
POZNÁMKA: V této sloučenině máme výskyt fenomén rezonance, ve kterém se elektrony ze dvou vazeb pí pohybují řetězcem. Pár elektrony pí začíná zaujímat centrální oblast řetězce (mezi uhlíky 2 a 3), zatímco elektrony z druhé vazby pí jsou posunuty na jeden z koncových uhlíků. Máme tedy vazebná místa na uhlících 1 a 4 a dvojnásobek mezi uhlíky 2 a 3.

Rezonance ve struktuře but-2,3-dienu
Na Diels-Alderova reakce, jedním z činidel je konjugovaný dien, zatímco druhým je organická sloučenina, která se může vyskytovat hovor dvojnásobek mezi atomy uhlíku. Níže je uveden příklad a Diels-Alderova reakce mezi but-2,3-dienem a propenem:
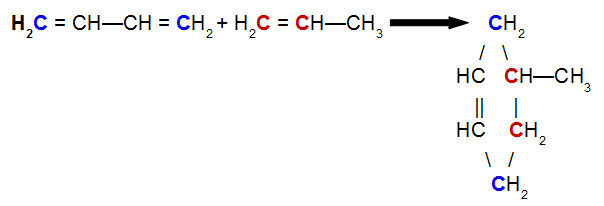
Rovnice Diels-Alderovy reakce but-2,3-dienu s propenem
Při analýze výše uvedené rovnice vidíme, že uhlíky 1 a 4 (oba modře) but-2,3-dienové vazby na uhlíky 1 a 2 (oba červené) propenu, což vede k rozvětvenému cyklenu, 4-methyl-cyklohexen. To je způsobeno rezonancí v molekule but-2,3-dienu, která posune vazbu pi mezi uhlíky 2 a 3, a zlomením vazby pi mezi uhlíky 1 a 2 propenu.
OBS.²: Je důležité zdůraznit, že bez ohledu na sloučeninu, která reaguje s konjugovaným alkadienem, dojde k přerušení vazby pí pouze mezi atomy uhlíku v řetězci. Pokud má struktura pi vazby mezi atomy jinými než uhlík, nerozbijí se. Níže je uveden příklad struktury, která může reagovat s a alkadien v Diels-Alderova reakce, což má za následek rozbití vazby pí mezi uhlíky (modře) dvojné vazby.
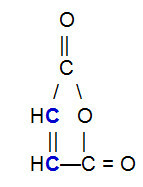
Strukturní vzorec anhydridu kyseliny maleinové
Podle mě. Diogo Lopes Dias
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/reacoes-diels-alder.htm