Při izotermické transformaci kolísání objemu a tlaku určitého plynu, ale konstantní teplota; odtud tedy původ izotermického názvu (řecky: iso = stejné; termo = teplo).
Vědci Boyle a Mariotte izolovaně provedli podobné experimenty a dosažený výsledek byl: se zvyšujícím se tlakem se zmenšuje objem plynu.
Pomysli například na píst injekční stříkačky. Pokud na tento píst použijeme vnější tlak, to znamená, že pokud tlak zvýšíme, sníží se objem vzduchu uvnitř injekční stříkačky a naopak.
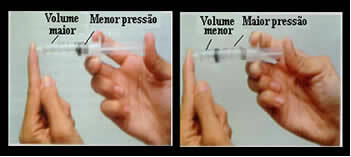
Objem a tlak jsou nepřímo úměrné: v levém poli je tlak malý a objem obsazený vzduchem je velký. Vpravo, když je na píst injekční stříkačky vyvíjen větší tlak, objem klesá.
Nejedná se o ojedinělý případ, jedná se o něco, co se opakuje s běžnou pravidelností pro plyny. Proto byla tato skutečnost uvedena ve formě zákona, který lze popsat následovně:
| Boyleův zákon nebo Boyle-Mariotteův zákon: Při konstantní teplotě je objem obsazený pevnou hmotou plynu nepřímo úměrný jeho tlaku. |
To znamená, že pokud zdvojnásobíme tlak plynu, jeho objem se sníží na polovinu atd. Jsou-li dvě taková množství nepřímo úměrná, jejich součinem je konstanta; tedy matematicky lze tento vztah vyjádřit takto:
| P.V = k |
Kde k = konstantní.
Pokud tedy máme v první situaci hodnotu tlaku určitého plynu jako P1 a jeho příslušný objem jako V1, pak musíme:
| P1. PROTI1 = k |
Pokud tento tlak zvýšíme na P2, změní se také jeho objem na V2 a znovu budeme muset:
| P2 . PROTI2 = k |
Docházíme tedy k závěru:
| P1. PROTI1 = P2. PROTI2 |
Tuto stálost lze vidět na příkladu v tabulce níže, tlaků a objemů plynu se stálou hmotností:
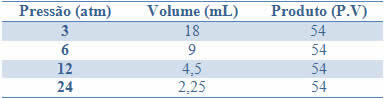
Grafem těchto hodnot uvidíme vytvoření křivky.
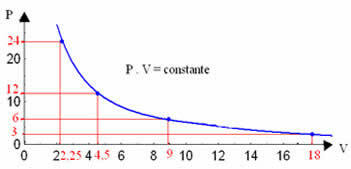
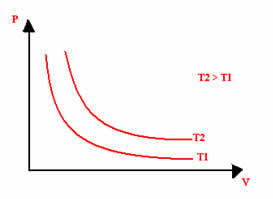
Grafické znázornění izotermické transformace bude vždy hyperbola, bez ohledu na hodnoty tlaku a objemu a teploty, při kterých byl experiment proveden. Tato hyperbola se nazývá izoterma; takže, jak je vidět na níže uvedeném grafu, různé teploty vedou k různým izotermám.
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/transformacao-isotermica-ou-lei-boyle.htm

