je nazýván iontový paprsek velikost iontu. Studium této vlastnosti závisí na znalostech o atomovém poloměru a iontech.
Atomový poloměr: je míra velikosti neutrálního atomu (teoretická vzdálenost od jádra k poslední elektrosféře).
ionty: atomy, které ztrácejí (kationty) nebo získávají elektrony (anionty).
Protony uvnitř jádra a atom vyvíjet přitažlivou sílu na elektrony (negativní částice) přítomné v elektro sférách. Čím větší je počet protonů, tím větší je tato přitažlivost a naopak. Když se počet elektronů v atomu změní ztrátou nebo ziskem těchto částic, přitažlivost mezi protony a elektrony se změní takto:
V případě kationu:
Počet elektronů v elektrosférách je menší než počet protonů uvnitř jádra, což zvyšuje přitažlivou sílu jádra a přitahuje elektrony blíže k ní. elektrosféry. Výsledkem je zmenšení poloměru atomu. Poloměr kationtu bude tedy vždy menší než poloměr jeho neutrálního atomu.
Poloměr neutrálního atomu> Poloměr kationtu
V případě aniontu:
Počet elektronů v elektrosférách je větší než počet protonů uvnitř jádra. V tomto případě je přitažlivá síla vyvíjená jádrem překonána odpudivou silou mezi elektrony přítomnými v elektro sférách, což má za následek zvětšení poloměru atomu. Poloměr anionu bude tedy vždy větší než poloměr jeho neutrálního atomu.
Poloměr anionu> Poloměr neutrálního atomu
Níže uvedené dvě situace jsou dobrým příkladem toho, co se stane s poloměrem iontu:
1) Neutrální atom sodíku (11Na) a kation sodný (11Na+)
Zatímco neutrální atom sodíku má jedenáct protonů (žluté koule) a jedenáct elektronů (červené koule), kation sodíku má jedenáct protonů a deset elektronů.

Model neutrálního atomu sodíku
Když neutrální atom sodíku ztratí elektron, poloměr se zmenší.
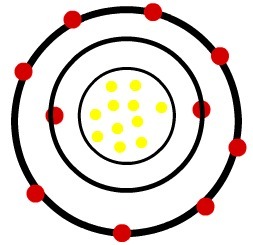
Model kationu sodíku
Pozorování: Třetí úroveň nebyla v obraze kationu zastoupena, protože protože ztratila jediný elektron, který měla, stala se prázdnou, a proto byla ignorována, ale je přítomna.
2.) Fosforový neutrální atom (15P) a kation fosforu (15P-3)
Zatímco atom neutrálního fosforu má patnáct protonů (žluté koule) a patnáct elektronů (červené koule), anion fosforu má patnáct protonů a osmnáct elektronů.
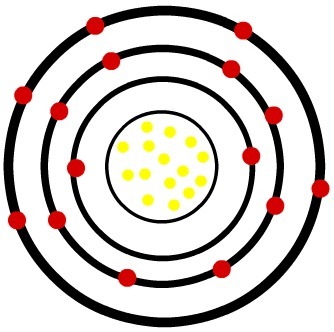
Model atomu neutrálního fosforu
Když atom neutrálního fosforu získá tři elektrony, poloměr se zvětší.
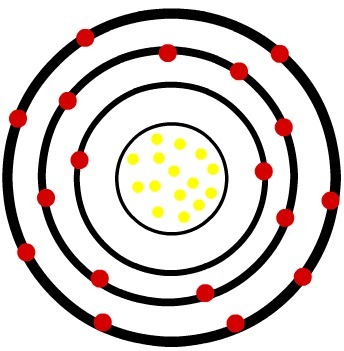
Model aniontu fosforu
Podle mě. Diogo Lopes Dias

