Bílý fosforje alotropní forma chemického prvku fosfor, běžně reprezentovaný molekulárním vzorcem P4. Přestože se mu říká bílý fosfor, jeho barva připomíná spíše vosk nebo nažloutlou. Bílý fosfor je považován za nejstabilnější formu fosforu, i když není termodynamicky nejstabilnější.
Bílý fosfor má málo přímých použití v průmyslu, je obecně přeměněn na červený allotrop, který má přímější použití a je méně toxický. Bílý fosfor se však používá ve vojenských konfliktech jako činidlo způsobující kouř, pro osvětlení a také k vytváření požárů, protože bílý fosfor se vznítí při kontaktu se vzduchem a při teplotách mírně vyšších než 30 °C.
Přečtěte si také: Jaké jsou alotropní formy síry?
Témata v tomto článku
- 1 - Shrnutí bílého fosforu
- 2 - Co je bílý fosfor?
- 3 - Složení bílého fosforu
- 4 - K čemu se používá bílý fosfor?
-
5 - Použití bílého fosforu ve válce
- → Bomba s bílým fosforem
- → Účinky expozice bílému fosforu
- 6 - Rozdíly mezi bílým fosforem a červeným fosforem
Shrnutí bílého fosforu
- Bílý fosfor je alotropní forma fosforu, reprezentovaná vzorcem P4.
- Má nažloutlou barvu, blízkou barvě vosku.
- Lze jej vyrábět z fosfátových hornin, písku a koksu při vysokých teplotách.
- Je velmi špatně rozpustný ve vodě a vznítí se při teplotách těsně nad 30°C.
- V průmyslu není široce používán, ale je hlavní elementární formou produkovaného fosforu.
- Používá se v konfliktech a válkách jako prostředek způsobující kouř, požáry a pro osvětlení.
- Má přímější použití než bílý fosfor a je také méně toxický než on.
Co je bílý fosfor?
Bílý fosfor je jednou z 12 alotropních forem, které existují chemický prvek fosfor, běžně zastupovaný jako P4.
Ve starověku byla moč jediným známým zdrojem prvku fosfor a proto všechny studie o tomto prvku odkazovaly na produkci z moči. Fosfor vyrobený v tomto procesu měl bílou (nebo nažloutlou, voskovitou) barvu, což způsobuje že bílý fosfor byl první alotropní formou tohoto prvku, která ho také zvýšila sláva.
zezadu, V druhé polovině 19. století bylo zjištěno, že bílý fosfor lze vyrábět zahříváním fosfátových hornins pískem a koksem. Tato metoda byla vylepšena pro moderní způsob výroby bílého fosforu, který spočívá v použití a elektrická pec (která dosahuje teplot v rozmezí 1 400 až 1 500 °C) pro ohřev fosfátové horniny (Tady3(PRACH4)2), písek (oxid křemičitý, SiO2) a koks (uhlík).
2Ca3(PRACH4)2 + 6 SiO2 + 10 C → P4 + 6 CaSiO3 + 10 CO
Páry fosforu kondenzují a tvoří voskovou pevnou látku, která je nerozpustná ve vodě.
Nepřestávej teď... Po reklamě je toho víc ;)
Složení bílého fosforu
Bílý fosfor je obvykle nejstabilnější formou fosforu, i když je ve skutečnosti metastabilní (jeho zahřívání vede k termodynamicky stabilnějším alotropním formám, červené a černé).
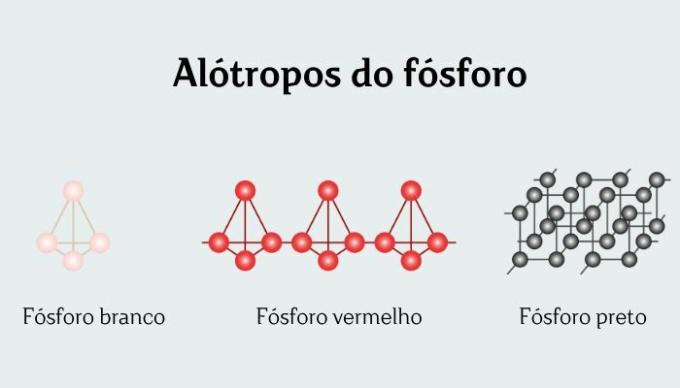
Objevuje se v krystalické formě jako molekuly P4 čtyřstěnný s P─P vazbami o délce rovné 221 pm. Je rozpustný v benzenu, PCl3 a C.S.2, velmi málo rozpustný ve vodě. Ve skutečnosti je bílý fosfor uložen ve vodě, aby se zabránilo jeho oxidaci.
Ve vlhkém vzduchu prochází chemiluminiscenční oxidací, vydává zelenou záři a pomalu se přeměňuje na P4Ó8 a3.
K čemu je dobrý bílý fosfor?
Bílý fosfor má široké využití ve vojenském průmyslu, jako výrobce kouře a pro plnění projektilů a granátů.
V průmyslu se obecně vyrábí jako elementární fosfor z fosfátových hornin, aby se pak přeměnil na červený fosfor, další alotropní forma, která má odlišné chemické chování. Červený fosfor má širší obecné použití, používá se k výrobě zápalek, fosfidu hliníku, zpomalovačů hoření a pro pyrotechnické účely. Bílý fosfor je také hlavním způsobem výroby sloučenin vyšší čistoty, které mohou obsahovat fosfor. Vyrábí také PCl3reakcí s Cl2.
Viz také: Koneckonců, je zápas v krabici nebo na hokejce?
Použití bílého fosforu ve válce
Bílý fosfor se nakonec používá pro vojenské účely, a to kvůli jeho samovznícení při nízkých teplotách: nad 50 °C (někteří autoři uvádějí nad 34 °C), při kontaktu se vzduchem se vznítí bílý fosfor a vzniká oxid fosforečný (P4Ó10).
→ Bomba s bílým fosforem
Bílý fosfor se vznítí při nízkých teplotách. Proto, použití bílého fosforu jako zápalné zbraně je v konfliktech běžné. Jeho použití není založeno na smrtelnosti, ale spíše k vytvoření ohně, osvětlení nebo dokonce kouřové clony na pomoc při útěku nebo ústupu jednotek. K tvorbě kouře dochází, když je teplota dostatečně vysoká ve vztahu k teplotě počátku samovznícení alotropní formy.

Protože existují již zmíněná použití bílého fosforu (osvětlení, kouřová clona a podpora ohně), mezinárodní úmluvy jeho použití v konfliktech nezakazují. Úmluva OSN o chemických zbraních (CWC) ji nepovažuje za chemickou zbraň. Jediným problémem je, že pokud by byl bílý fosfor použit k přímému zapalování lidí na civilní cíle, mohl by porušovat protokol III Úmluvy o některých konvenčních zbraních (CCCW). Tuto skutečnost by však bylo nutné prokázat šetřením ze strany příslušných orgánů.
→ Účinky expozice bílému fosforu
Jakmile se oheň bílého fosforu zapálí, je těžké ho uhasit. Velmi snadno přilne k pokožce a oděvu, což způsobuje výrazné popáleniny. Navíc i po počátečním ošetření se může bílý fosfor znovu vznítit, pokud je stále v kontaktu se vzduchem. Proto je nezbytné odstranit jakékoli stopy fosforu z ran.
Nejprve je nezbytné mytí vodou a solnými roztoky, protože to může nejen snížit teplota, stejně jako zastavení spalování a odstranění všech stop zředěné kyseliny fosforečné, které mohou mít byla vytvořena. Absorpce fosforu popálením může způsobit odchylky v hladinách vápníku a fosforu v těle, které mohou rychle vytvářet hypokalcémie a hyperfosfatémie, což může být příčinou fatální srdeční arytmie.
Kouř extrémně dráždí sliznice, kde se spojuje s vodou za vzniku kyseliny fosforečné. Vdechování kouře bílého fosforu způsobuje podráždění dýchacích cest, generování kašle, bolesti hlavy a opožděného plicního edému.
Bílý fosfor je pro člověka velmi toxický a rychle se vstřebává do krve a jater. Požití 100 mg může být smrtelné v důsledku selhání jater. Pomalé, dlouhodobé vystavení malým množstvím také způsobuje hrozné následky. Nejčastější stav je zápasová čelist, která na konci 19. a na počátku 20. století postihla několik dělníků ve fosforových továrnách.
Rozdíly mezi bílým fosforem a červeným fosforem
Bílý a červený fosfor jsou různé alotropní formy chemického prvku fosfor, oba zastoupeni P4.
Červený fosfor lze získat z bílého fosforu zahříváním v inertní atmosféře na teplotu v rozmezí 540 K (267 °C). Poprvé jej získal Anton von Schötter v roce 1845.
Existuje několik krystalických forem červeného fosforu. Jedním z nich je Hittorf (také známý jako fialový fosfor), který se skládá z dlouhého a složitého fosforového řetězce.
Červený fosfor je méně hustý než bílý, má vyšší bod tání a je méně reaktivní. Kromě toho se červený fosfor také nepovažuje za toxický, což usnadňuje a usnadňuje manipulaci.
Prameny
CHOU, T.-D.; LEE, T.-W.; CHEN, S.-L.; TUNG, Y.-M.; DAI, N.-T.; CHEN, S.-G.; LEE, C.-H.; CHEN, T.-M.; WANG, H.-J. Řízení spalování bílého fosforu. popáleniny, n. 27, str. 492-497, 2001.
HOUSECROFT, C. A.; SHARPE, A. G. Anorganická chemie. 2. vyd. Pearson Education Limited: Londýn, 2005.
Kelly, P. F. Fosfor: Anorganická chemie. V: Encyklopedie anorganické chemie. 2. vyd. Wiley: New Jersey, 2005.
SVĚTOVÁ ZDRAVOTNICKÁ ORGANIZACE. Bílý fosfor. Světová zdravotnická organizace, 20. října. 2023. K dispozici v: https://www.who.int/news-room/fact-sheets/detail/white-phosphorus.
Chtěli byste odkazovat na tento text ve školní nebo akademické práci? Dívej se:
NOVAIS, Stéfano Araújo. "Bílý fosfor"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/fosforo-branco.htm. Zpřístupněno 9. listopadu 2023.
