A druhý zákon termodynamiky určuje, jaké podmínky pro to existují teplo být přeměněn na práci v tepelných motorech a chladničkách. Zabývá se také definicí entropie jako jev schopný měřit dezorganizaci částic ve fyzikálních systémech.
Přečtěte si také: Kalorimetrie — obor fyziky, který studuje výměnu tepla
Témata tohoto článku
- 1 - Shrnutí druhého termodynamického zákona
- 2 - Jaký je druhý termodynamický zákon?
-
3 - Aplikace druhého zákona termodynamiky
- Druhý zákon termodynamiky tepelných motorů
- Druhý termodynamický zákon v ledničkách
- 4 - Entropie a druhý termodynamický zákon
-
5 - Vzorce 2. termodynamického zákona
- Tepelné stroje a chladničky
- Ledničky
- Příklady použití vzorců
- 6 - Carnotův cyklus
- 7 - Zákony termodynamiky
- 8 - Řešené úlohy z druhého termodynamického zákona
Shrnutí druhého termodynamického zákona
Druhý termodynamický zákon představují Clausiovy a Kelvin-Planckovy výroky.
Clausiův výrok se zabývá tokem tepla z teplejšího tělesa do chladnějšího tělesa.
Kelvin-Planckovo prohlášení se zabývá neschopností tepelných zařízení přeměnit veškeré své teplo na práce.
Druhý termodynamický zákon je aplikován na tepelné motory a chladničky.
Carnotův cyklus je cyklus maximální účinnosti dosažený tepelnými motory.
Carnotův cyklus má čtyři stupně, vratnou izotermickou expanzi, vratnou adiabatickou expanzi, vratnou izotermickou kompresi a vratnou adiabatickou kompresi.
Carnotova věta se vztahuje k výnosu Carnotovy stroje.
Jaký je druhý termodynamický zákon?
Druhý termodynamický zákon je a zákon, který řeší omezení, která se vyskytují v termodynamických procesech. Prohlásili to fyzici Rudolf Clausius (1822-1888), Lord Kelvin (1824-1907) a Max Planck (1858-1947), jak uvidíme níže:
Fyzik a matematik Rudolf Clausius uvedl, že k vedení toku tepla dochází z tělesa s vyšší teplotou do tělesa s nižší teplotou. nižší teplota, proto není přirozené, aby docházelo k inverznímu procesu, proto je nutné na tom pracovat Systém. S tím prohlásil:
Je nemožné provést proces, jehož jediným účinkem je přenos tepla z chladnějšího tělesa na teplejší těleso.|1|
Matematický fyzik William Thomson, známý jako Lord Kelvin, spolu s příspěvky fyzika Maxe Plancka, konstatovala nemožnost tepelných zařízení s účinností 100%, protože tepelné ztráty budou vždy.
Nepřestávej teď... Po publicitě je toho víc ;)
Aplikace druhého zákona termodynamiky
Druhý termodynamický zákon je aplikován na tepelné motory a chladničky.
Druhý zákon termodynamiky ve strojích tepelný
K Tepelné stroje jsou schopny přeměnit teplo na práci. Horký zdroj dodává teplo tepelnému motoru, který jej přeměňuje v práci. Zbytek tepla odešle do zdroje chladu, jak je znázorněno na obrázku níže:
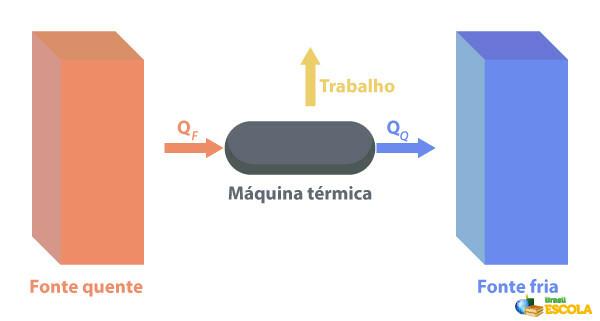
Některé příklady tepelných strojů jsou: parní a petrolejové turbíny v proudových letadlech, spalovací motory, termonukleární reaktory.
Druhý termodynamický zákon v ledničkách
Chladničky jsou stroje, které Pracují opačně než tepelné motory., kde odvádějí teplo z regionu s teplota nižší teplotu a dodávat jej do oblasti s vyšší teplotou. Protože to není přirozené, je nutné, aby stroj vykonával práci s využitím elektrické energie, jak je popsáno na obrázku níže:
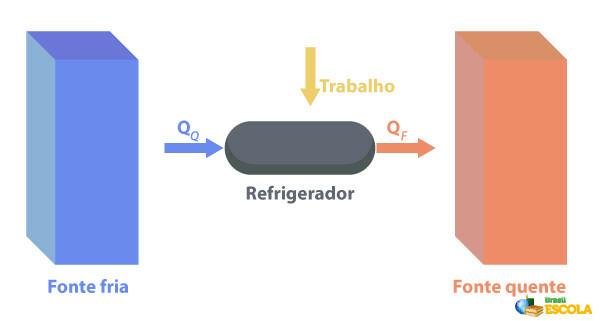
Některé příklady chladniček jsou chladničky a klimatizace.
Entropie a druhý termodynamický zákon
A druhý zákon termodynamiky navrhuje existenci entropie, jeden Fyzické množství odpovědné za měření stupně dezorganizace částic ve fyzikálním systému nebo stupně nevratnosti termodynamické procesy probíhající v tepelných motorech, které jsou spontánní, nevyhnutelné, nevratné a expanzivní. S tím je možné pouze pozorovat a kontrolovat stupeň volatility procesů. Se zvyšující se entropií se zvyšuje i stupeň neuspořádanosti v systému.
A Nomenklatura entropie je řeckého původu a znamená „transformace“., „změnit“, takže se používá v Fyzický k označení náhodnosti a neuspořádanosti. Entropii lze vypočítat pomocí vzorce:
\(∆S=\frac{∆U}T\)
\(∆S\) je změna entropie, měřená v [J/K].
\(∆U\) je změna vnitřní energie, měřená v joulech [J].
T je teplota měřená v Kelvinech [K].
Ze statistického hlediska se entropie vypočítá podle vzorce:
\(S=k\cdot ln\ Ω\)
S je entropie, měřená v [J/K].
k je Boltzmannova konstanta, stojí za to \(1,4\cdot 10^{-23}\ J/K\).
Ω je počet možných mikrostavů pro systém.
Přečtěte si také: Procesy šíření tepla
Vzorce druhého termodynamického zákona
Tepelné stroje a chladničky
\(Q_Q=W+Q_F\)
\(Q_Q\) je teplo horkého zdroje, měřené v joulech [J].
W je práce vykonaná tepelným motorem, měřená v joulech [J].
\(Q_F\) je teplo ze zdroje chladu, měřené v joulech [J].
Může být reprezentován:
\(W=Q_Q-Q_F\)
W je práce vykonaná tepelným motorem, měřená v joulech [J].
\(Q_Q\) je teplo horkého zdroje, měřené v joulech [J].
\(Q_F\) je teplo ze zdroje chladu, měřené v joulech [J].
Ledničky
\(η=\frac{Q_F}{Q_Q-Q_F}\)
\(η\) je účinnost chladničky.
\(Q_F\) je teplo ze zdroje chladu, měřené v joulech [J].
\(Q_Q\) je teplo horkého zdroje, měřené v joulech [J].
Může být reprezentován jako:
\(η=\frac{Q_F}W\)
\(η\) je účinnost chladničky.
\(Q_F\) je teplo ze zdroje chladu, měřené v joulech [J].
W je práce vykonaná tepelným motorem, měřená v joulech [J].
Příklady aplikace vzorců
Příklad 1: Vypočítejte práci, kterou vykoná tepelný stroj během cyklu, kdy přijme 500 J tepla z horkého zdroje a předá pouze 400 J tepla studenému zdroji.
Pro výpočet práce tepelného motoru použijeme vzorec:
\(W=Q_Q-Q_F\)
Nahrazení hodnot uvedených v příkazu:
\(W=500-400\)
\(W=100\ J\)
Práce tepelného motoru byla 100 joulů.
Příklad 2: Jaká je účinnost chladničky, která přijme 150 J tepla z teplého zdroje a předá 50 J tepla studenému zdroji?
Pro výpočet účinnosti chladničky použijeme vzorec:
\(η=\frac{Q_F}{Q_Q-Q_F}\)
Nahrazením hodnot uvedených v příkazu získáme:
\(η=\frac{50}{150-50}\)
\(η=\frac{50}{100}\)
\(η=0,5\)
Vynásobení výnosu 100%:
\(η=0,5\cdot100%\)
\(η=50\%\)
Chladnička má 50% účinnost.
Carnotův cyklus
Carnotův cyklus byl vyvinul vědec Sadi Carnot (1796-1832), s cílem identifikovat maximální účinnost, které může být dosaženo tepelným motorem, který pracuje mezi horkým zdrojem a studeným zdrojem.
Na základě svých studií Carnot zjistil, že pro dosažení maximální účinnosti tepelného motoru ano nezbytný k tomu, aby byl jeho proces reverzibilní, a tak vyvinul cyklus maximálního výnosu zvaný cyklus of Carnot a Tepelný stroj, který přes něj pracuje, se nazývá Carnotův tepelný stroj.. Vzhledem k tomu, že Carnotův cyklus je reverzibilní, lze jej obrátit, a tak byly vyvinuty chladničky.
Carnotův cyklus, bez ohledu na použitou látku, se skládá ze čtyř procesů popsaných v grafu tlak podle objemu (p×V), jak můžeme vidět na obrázku níže:
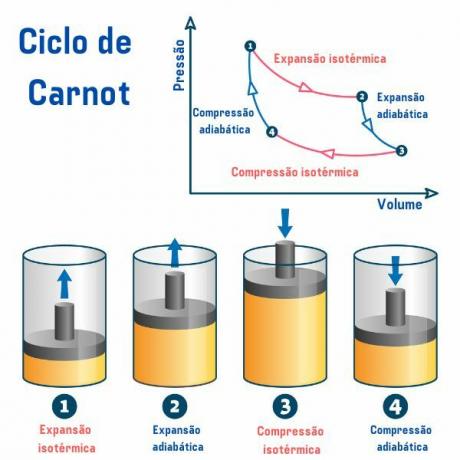
1. postup, z bodu 1 → 2: dochází k reverzibilní izotermické expanzi (proces, při kterém teplota zůstává konstantní), při kterém plyn (nebo systém) pracuje a získává určité množství tepla z horkého zdroje.
2. postup, z bodu 2 → 3: dochází k adiabatické expanzi (proces, při kterém dochází k výměně tepla s vnějším prostředím) vratné, při které nedochází k výměně tepla tepla s tepelnými zdroji, ale plyn funguje a dochází k poklesu jeho vnitřní energie, což způsobuje pokles v teplota.
3. postup, od bodu 3 → 4: dochází k reverzibilní izotermické kompresi, při které plyn přijímá práci a předává množství tepla zdroji chladu.
4. proces, od bodu 4 → 1: dochází k reverzibilní adibatické kompresi, při které nedochází k výměně tepla s tepelnými zdroji a plyn ano ohřívá, dokud nedosáhne teploty horkého zdroje, a tak se s ním dostane do kontaktu a skončí cyklus.
zákony termodynamiky
Zákony termodynamiky jsou čtyři zákony, které řídí celé studium termodynamika, studovat vztahy mezi objemem, teplotou a tlakem a dalšími fyzikálními veličinami, jako je teplo a energie.
Nultý zákon termodynamiky: je zákon tepelná bilance, studuje výměnu tepla mezi tělesy, která mají různé teploty.
první zákon termodynamiky: je zákon zachování energie v termodynamických systémech, studuje přeměnu tepla na práci a/nebo vnitřní energii.
Druhý zákon termodynamiky: je to zákon, který se zabývá tepelnými motory, ledničkami a entropií.
Třetí zákon termodynamiky: je zákon absolutní nula, studuje účinky této teploty.
Čtěte také: Výkon tepelných motorů
Řešené úlohy z druhého termodynamického zákona
Otázka 1 Určete teplotu horkého zdroje Carnotova motoru s vědomím, že teplota studeného zdroje je 450 K a jeho účinnost je 80 %.
a) 2250 K
b) 450 tis
c) 1500 tis
d) 900 tis
e) 3640 K
Rozlišení:
Alternativa A. Teplotu horkého zdroje vypočítáme na základě vzorce účinnosti Carnotova motoru:
\(η=1-\frac{T_F}{T_Q} \)
\(80 \%=1-\frac{450}{T_Q} \)
\(\frac{80}{100}=1-\frac{450}{T_Q} \)
\(0,8=1-\frac{450}{T_Q} \)
\(0,8-1=-\frac{450}{T_Q} \)
\(-0,2=-\frac{450}{T_Q} \)
\(0,2=\frac{450}{T_Q} \)
\(T_Q=\frac{450}{0,2}\)
\(T_Q=2250\ K\)
otázka 2 (Cefet-PR) 2. princip termodynamiky lze konstatovat takto: „Nelze postavit stroj tepelná energie pracující v cyklech, jejímž jediným účinkem je odebírat teplo ze zdroje a integrálně ho přeměňovat práce". Tento princip nás dále vede k závěru, že:
a) Vždy je možné postavit tepelné stroje, jejichž účinnost je 100 %.
b) každý tepelný stroj potřebuje pouze jeden zdroj tepla.
c) teplo a práce nejsou homogenní veličiny.
d) jakýkoli tepelný stroj odebírá teplo z horkého zdroje a část tohoto tepla odvádí do studeného zdroje.
e) pouze se zdrojem chladu, udržovaným vždy na 0 °C, by bylo možné, aby určitý tepelný stroj přeměnil teplo zcela na práci.
Rozlišení:
Alternativa D. Tento princip nás informuje, že není možné odebrat veškeré teplo z horkého zdroje a přenést ho do studeného zdroje.
Poznámka
|1| Základní kurz fyziky: Tekutiny, Kmity a vlny, Teplo (sv. 2).
Autor: Pamella Raphaella Melo
Učitel fyziky
Entropie systému není nic jiného než míra jeho stupně dezorganizace. Druhý zákon je možné formulovat z pojmu entropie.
Objevte fascinující historii tepelných motorů a jejich hlavní použití.
Víte, co jsou tepelné stroje, termodynamické cykly a účinnost? Zjistěte více o těchto důležitých termodynamických konceptech.
Projděte si text a naučte se definici prvního zákona termodynamiky, podívejte se, jaké vzorce tento zákon používá, a podívejte se na vyřešená cvičení na toto téma.
Izotermická, izovolumetrická a adiabatická transformace. Potkat je!
Víte, co je termodynamika? Projděte si text a zjistěte, které jsou nejdůležitější pojmy na toto téma, seznamte se se zákony termodynamiky.

