V tomto textu uvidíme, jak a tabulka změna fyzického stavu každému čistá látka, jak interpretovat tento typ diagramu a jak je znázorněn graf směsí.
Podívejme se na příklad vody. Představte si, že vezmeme sklenici ledu o teplotě –10 ° C a zahájíme proces ohřevu pod tlakem 1 atm. Jak teplota stoupá od -10 ° C do -9 ° C, do -8 ° C atd., Zůstane led v pevném stavu, dokud nedosáhne teploty 0 ° C.
V tomto bodě se začíná měnit do kapalného stavu, to znamená, že začíná probíhat fúze. Teplota se nebude nadále zvyšovat jako dříve, ale zůstane konstantní na 0 ° C, dokud se nerozpustí veškerý led:

Po roztavení veškeré pevné látky se teplota systému bude nadále zvyšovat až do dosažení teploty 100 ° C. Při této teplotě se voda, která byla v kapalném stavu, začne měnit na parní, to znamená, že bude vřít.
Stejně jako se to stalo v fúzní bodpři teplotě varu také teplota zůstane konstantní, dokud se veškerá kapalina nezmění na páru. Poté, pokud budeme systém neustále zahřívat, bude teplota stále stoupat:
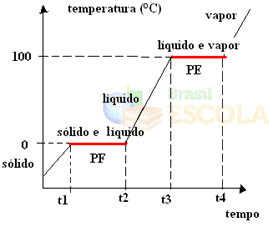
Připraven! Toto je graf nebo diagram, který představuje změnu fyzikálního stavu vody nebo její topné křivky. Pokud by to byl inverzní proces, měli bychom následující křivku vodního chlazení:
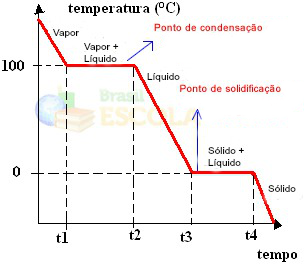
Velmi důležitým aspektem těchto grafů je, že jsou tvořeny dvěma úrovněmi, to znamená, že existují dva body, kde teplota na chvíli zůstává konstantní. K tomu vždy dochází při změně stavu čisté látky. Jediným rozdílem jsou hodnoty bodu tání a bodu varu.
Například kyslík, na rozdíl od vody, není kapalina, ale plyn při pokojové teplotě (asi 20 ° C). Je to proto, že jeho bod tání na hladině moře je -223,0 ° C a jeho bod varu je -183,0 ° C. Podívejte se na graf změn svého fyzického stavu:

Běžná grafika mixu
Pokud zahříváme nebo ochlazujeme směs, nebude mít bod tání a bod varu stanovené a konstantní hodnoty, tj. dvě úrovně pozorované v grafech, nebudou vytvořeny výše.
Ke změnám fyzikálních stavů dojde spíše v teplotních rozsazích, než v pevném množství. Například teplota tání začíná při dané teplotě a končí při jiné teplotě a totéž se stane s bodem varu, jak ukazuje následující graf:
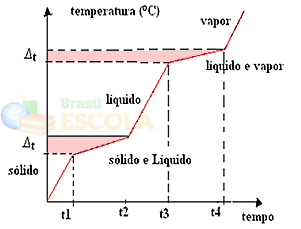
Dvě výjimky jsou eutektické a azeotropické směsi. Podívejte se, co se s nimi stane:
a) Eutektická směs
Eutektická směs se během fúze chová, jako by to byla čistá látka, to znamená, že v tomto bodě zůstává teplota konstantní od začátku do konce změny stavu agregace.

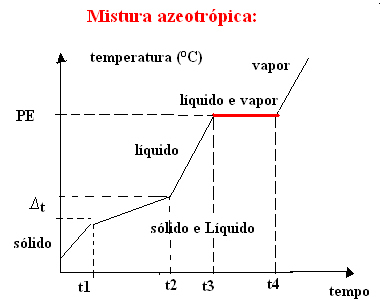
b) azeotropní směs
Azeotropická směs se během varu chová jako čistá látka, to znamená, že v tomto bodě zůstává teplota konstantní od začátku do konce změny stavu agregace.
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/graficos-mudanca-estado-fisico.htm
