Obvykle reakce vodná elektrolýza a magmatická elektrolýza provádějí se grafitovými a platinovými elektrodami, které se neúčastní reakce; vedou pouze elektrický proud. Existují však některé konkrétní případy, kdy je nutné použít aktivní elektrody, tj. které procházejí redukcí a oxidací.
Hlavní případy použití těchto elektrod, které se účastní redoxního procesu, jsou: a elektrolytické čištění kovů, jako je zinek, kobalt, nikl a zejména měď; a také galvanické pokovování. Podívejme se, jak k jednotlivým případům dochází:
• Měděné elektrolytické čištění: tato elektrolytická rafinace mědi může produkovat čistotu asi 99,9% a používá se hlavně k výrobě měděné dráty, které, pokud mají co nejméně nečistot, mohou mít schopnost vést velmi elektrický proud zmenšil.
Podívejte se, jak tento proces probíhá, a podívejte se na schéma elektrolytické vany sestavené níže:

Potenciální rozdíl je aplikován na vodný roztok síranu měďnatého (CuSo4 (aq)) - který vede elektřinu - takže anoda, která je nečistá kovová měď, ztrácí elektrony, to znamená, že podléhá oxidaci a uvolňuje své kationty (Cu
2+), které jsou uloženy na negativní desce. Může to být inertní platinová deska nebo, lépe, čistá měděná deska. Představuje katodu, která se redukuje, protože se v ní usazuje měď. Takže semireakce, které se vyskytují v elektrodách, jsou: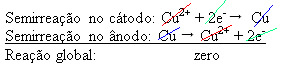
Skutečnost, že poskytla nulový výsledek, naznačuje, že nedošlo k žádné chemické reakci, ale pouze k transportu mědi. Na dně nádoby jsou další nečisté látky, které byly v mědi, jako je zlato, stříbro, oxid křemičitý (písek) a další minerály, které lze dokonce prodávat.
• Galvanické pokovování: na materiál, který má být chráněn před korozí, se nanese kovový povlak.
Kov vybraný pro povlak - který může být chrom (chromování), nikl (niklování), stříbro (stříbrné pokovování), zlato (zlacení) nebo zinek (galvanizace) - bude anoda, kladná elektroda, která prochází oxidací a ztrácí elektrony. Místo materiálu, který byl chráněn, prochází oxidací, protože jeho redukční potenciál je větší.
Záporná elektroda, tj. Katoda, která přijímá tyto elektrony a prochází redukcí, je samotný materiál, který byl potažen. Tímto způsobem zůstává chráněn, i když je jeho povrch nějak narušen.
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/eletrolise-com-eletrodos-ativos.htm