Zvažte obecnou reverzibilní reakci níže, kde malá písmena odpovídají vyváženým reakčním koeficientům a velká písmena jsou reaktanty a produkty jsou všechny plynné:

S ohledem na každý z reakčních směrů samostatně, jejich rychlosti vývoje (Td) jsou dány vztahem:
* Přímá reakce: aA + bB → cC + dD
VšechnoPřímo = K.Přímo. [THE]The. [B]B
* Reverzní reakce: cC + dD → aA + bB
Všechnoinverzní = K.zvrátit. [C]C. [D]d
Chemická rovnovážná konstanta z hlediska koncentrace v množství hmoty (K.C) a z hlediska parciálního tlaku (K.P) bude dáno dělením KPřímo autor: K.zvrátit.
Takže máme:
K.Přímo. [THE]The. [B]B = 1 → K.Přímo__ = __[C]C. [D]d___
K.zvrátit. [C]C. [D]d K.zvrátit [THE]The. [B]B
Být, K.C =_KPřímo_
K.zvrátit
Takže máme:
K.C =__[C]C. [D]d___ nebo K.P =__(Praça)C. (pD)d___ |
Kde p je parciální tlak každé látky v rovnováze.
Tímto způsobem se každá koncentrace zvýší na exponent odpovídající koeficientu příslušné látky v reakci a KC nemá jednotku *.
Kromě toho je velmi důležité zdůraznit, že v tomto výrazu
neměly by být zastoupeny pevné složky ani čisté kapaliny., protože na tomto výrazu se podílejí pouze záležitosti, které mohou trpět variací. Koncentrace v množství látky látky v pevném stavu je konstantní, a proto je již zahrnuta v hodnotě samotného K.C. Totéž platí pro čisté kapaliny, jako je voda. Ve zkratce, na expresi se podílejí pouze látky v plynném stavu a ve vodném roztoku.Všimněte si níže uvedených příkladů:
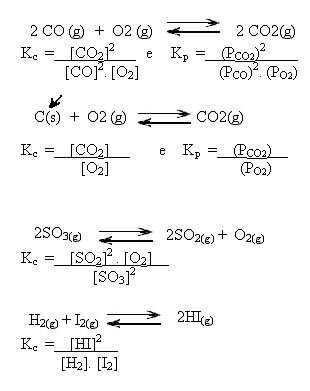
Hodnoty K.C může nám ukázat, zda je koncentrace reaktantů a produktů stejná nebo zda je jedna větší než druhá:
- -li K.C nebo K.P se rovná jedné (K.C = 1), to znamená, že koncentrace činidel a produktů je stejná;
- pokud je hodnota K.C nebo K.P být vysokýTo znamená, že produkty jsou ve větší koncentraci, protože ve vyjádření K.C produkty jsou v čitateli;
- pokud je hodnota K.C nebo K.P je nízký, to znamená, že činidla jsou ve vyšší koncentraci, protože v expresi K.C činidla jsou ve jmenovateli.
* K.C a K.P jsou to bezrozměrná čísla, tj. čistá čísla, bez jednotek souvisejících s jakoukoli velikostí nebo vztahem mezi veličinami.
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/constantes-equilibrio-kc-kp.htm
