K kyslíková funkce jsou skupinou organické sloučeniny které mají atomy kyslíku připojené k uhlíkovému řetězci. Jsou oni:
alkohol;
keton;
aldehyd;
karboxylová kyselina;
ester;
éter.
Přečtěte si také:Uhlovodíky – sloučeniny tvořené uhlíkem a vodíkem
Shrnutí funkce kyslíku
Kyslíkové funkce jsou skupinou sloučenin, které obsahují atom kyslíku. kyslík připojen přímo k uhlíkovému řetězci.
Různé funkce kyslíku se vyznačují specifickým strukturním uspořádáním atomy, nazývaná funkční skupina.
Funkční skupiny jsou zodpovědné za vlastnosti každé organické funkce.
Kyslíkové funkce jsou: alkohol, keton, aldehyd, karboxylová kyselina, ester a ether.
Video lekce o funkci kyslíku
Jaké jsou funkce kyslíku?
Funkce okysličeného těla jsou ty, které mají atom kyslíku navázaný na atom kyslíku uhlík uhlíkového řetězce.
Funkce kyslíku jsou:
alkohol;
keton;
aldehyd;
karboxylová kyselina;
ester;
éter.
Organické funkce jsou identifikovány svou funkční skupinou, což je strukturní uspořádání atomů nebo vazeb, odpovědné za charakteristické vlastnosti této sady sloučenin.
Význam kyslíkových funkcí
Přítomnost kyslíkových funkcí v organických sloučeninách je schopen měnit vlastnosti sloučeninve srovnání s příslušným uhlovodíkem se stejným počtem uhlíků.
Kyslíkové funkce jsou charakterizovány výskytem hydroxylových, karbonylových nebo karboxylových skupin. A přítomnost atomu kyslíku zvyšuje polární charakter sloučenin, čímž jsou hydrofilnější, to znamená, že se zvyšuje jejich afinita k voda.
Výskyt kyslíkových funkcí je také zodpovědný za typ mezimolekulární sílapůsobící mezi molekulami. Povaha a intenzita mezimolekulárních sil ovlivňují rozpustnost a teploty tání a varu.
Níže uvedená tabulka přináší srovnání některých vlastností tří sloučenin, které mají stejný počet atomů uhlíku, ale liší se přítomností okysličených funkčních skupin.
Organický kompost | |||
Butan (C4H10) |
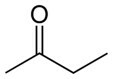
Butanon (C4H8Ó) |
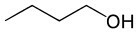
Butanol (C4H10Ó) |
|
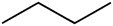 |
 |
 |
|
organická funkce |
Uhlovodík |
keton (kyslíková funkce) |
Alkohol (kyslíková funkce) |
Polarita |
nepolární |
Polární |
Polární |
teplota tání |
-138,3 °C |
-86 °C |
-89 °C |
teplota varu |
-0,5 °C |
80 °C |
118 °C |
Převládající mezimolekulární síla |
Indukovaný dipól |
permanentní dipól |
Vodíkové vazby |
Alkohol
Alkohol s organickou funkcí má hydroxylovou skupinu (-OH) vázanou přímo na nasycený uhlík, tedy atom uhlíku, který vytváří pouze jednoduché vazby.
Funkční skupina alkoholů: R-OH (hydroxyl).
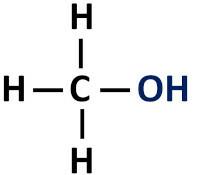
alkoholy jsou klasifikovány podle typu uhlíku, ke kterému je hydroxyl připojen. Primární alkoholy mají hydroxyl připojený k primárnímu uhlíku. Sekundární alkoholy mají hydroxylovou skupinu připojenou k sekundárnímu uhlíku a terciární alkoholy mají svou -OH skupinu připojenou k terciárním uhlíkům.
Organická sloučenina, která má pouze jeden hydroxyl, se nazývá monoalkohol. Pokud má dvě hydroxylové skupiny, nazývá se dialkohol. Nad tím se molekuly nazývají polyalkoholy.
A nomenklatura pro alkoholy následuje doporučení Iupac (International Union of Pure and Applied Chemistry), zvažuje sestavení názvu chemických struktur do tří částí:
Předpona – souvisí s počtem uhlíků.
Infix – označuje typ chemické vazby vytvořené mezi atomy uhlíku.
Přípona – souvisí s funkční skupinou. V případě alkoholů se používá přípona je -Ahoj.
Viz příklady:
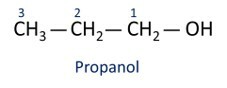
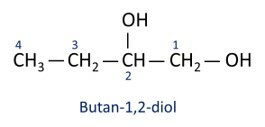
Ó hlavní alkohol je etanl (CH3CH2OH), používá se jako palivo, v alkoholických nápojích, jako chemické rozpouštědlo, čisticí a dezinfekční prostředek.
keton
Funkce organického ketonu odpovídá karbonylová funkční skupina (C=O), umístěná mezi dvěma atomy uhlíku uhlíkového řetězce.
Funkční skupina ketonů: R1-(C=O)–R2.

Ketony jsou klasifikovány podle počtu karbonylových skupin:
Monoketony – mají jednu karbonylovou skupinu.
Diketony – mají dvě karbonylové skupiny.
Polytony – mají více než dvě karbonylové skupiny.
A nomenklatura pro ketony se řídí pravidly Iupac, ale s rozdílem v pravopisu přípony. Ketony jsou identifikovány podle přípony -na.
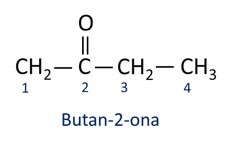
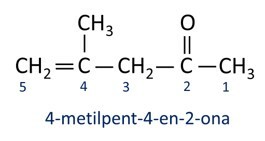
Obecně platí, že ketony nacházejí uplatnění při výrobě jiných chemikálií a léčiv. V průmyslu se ketony používají jako rozpouštědla pro barvy, barviva a laky. Jedním z nejznámějších ketonů je propanon, který je lidově známý jako aceton. K odstranění laku na nehty se používají roztoky acetonu.
Přečtěte si také:Amidy — sloučeniny, které mají na karbonyl navázaný dusík
Aldehyd
Organická aldehydová funkce je vyznačující se přítomností karbonylové funkční skupiny, jehož atom uhlíku má vodíkovou vazbu.
Funkční skupina aldehydů: H–C=O (formyl).
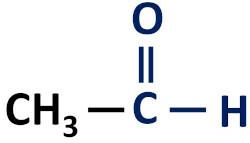
Aldehydy se vždy vyskytují na konci uhlíkových řetězců, protože jejich atom uhlíku musí být navázán alespoň na jeden atom vodíku.
A nomenklatura pro aldehydové sloučeniny řídí se pravidly IUPAC, liší se příponou. Aldehydy jsou identifikovány podle přípony -al.
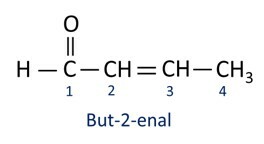
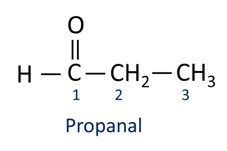
Aldehydy se průmyslově používají při výrobě parfémů a příchuť, protože jeho vůně a chuť se liší podle délky uhlíkového řetězce. Aldehydové sloučeniny se mimo jiné používají také při výrobě čisticích prostředků, léků, polymerů. Aldehydy s krátkým uhlíkovým řetězcem lze použít jako konzervační činidlo, jako je slavný formalín, což je aldehyd pojmenovaný methanal.

karboxylová kyselina
Funkční skupina organické karboxylové kyseliny je identifikována přítomností karboxylové funkční skupiny (-COOH).
Funkční skupina karboxylových kyselin: –(C=O)OH nebo –COOH.

Sloučeniny patřící do této organické funkce jsou slabé kyseliny, protože snadno uvolňují H ionty+ ve vodném roztoku.
A nomenklatura pro karboxylové kyseliny dodržuje pravidla IUPAC, nicméně termín „kyselina“ se objevuje před předponou, která označuje číslo uhlíku, a použitá přípona je -oic.
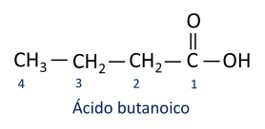
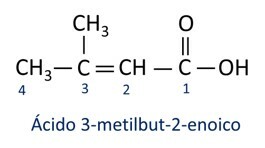
Ó nejběžnější karboxylová kyselina v každodenním životě je Octová kyselina, látka přítomná v octě. Vitamin C, hojný v mnoha citrusových plodech, je organická molekula zvaná kyselina askorbová.
Ester
Organická esterová funkce je identifikován přítomností karbonylové funkční skupiny, jehož atom uhlíku má kyslíkový ligand.
Funkční skupina esterů: –R–(C=O)O–R'.
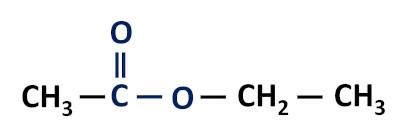
Estery jsou deriváty karboxylových kyselinLiší se od nich tím, že mají alkylový radikál připojený k atomu kyslíku namísto atomu vodíku.
Molekuly patřící do esterové funkce se tvoří reakcí mezi karboxylovou kyselinou a alkoholem, reakcí známou jako esterifikace.
Pravidla pro nomenklatura esterů definované Iupacem se domnívají, že molekula je tvořena dvěma částmi:
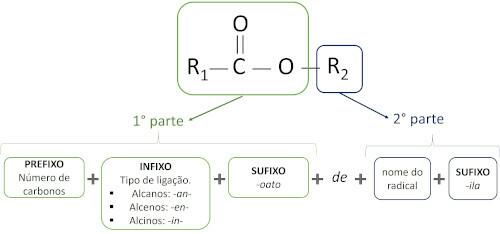
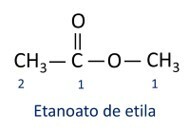
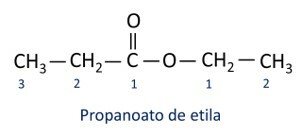
Hlavní charakteristikou esterů je jejich schopnost simulovat chuť a vůni přirozených potravin, podle délky uhlíkových řetězců (R1 a R2). Z tohoto důvodu se estery široce používají jako ochucovadla v potravinářském průmyslu, při výrobě léčiv, parfémů a kosmetiky.
Éter
Organická funkce etheru je vyznačující se tím, že má atom kyslíku mezi dvěma uhlíkovými řetězci.
Funkční skupina etherů: R–O–R.

Étery jsou vysoce hořlavé látky, s charakteristickým a silným zápachem.
A oficiální Iupac nomenklatura pro étery následuje předpona pořadí + infix + přípona. Strana molekuly, která má nejméně uhlíků, však obdrží příponu -oxy, zatímco delší uhlíkový řetězec je pojmenován, jako by to byl uhlovodík, který obdrží příponu -o.
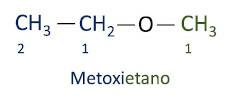
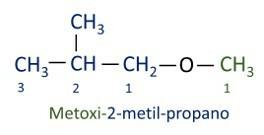
Étery jsou používá se jako rozpouštědla pro barvy, pryskyřice, oleje a tuky. V důsledku toho se používají v různých průmyslových a farmaceutických procesech. Éter se kdysi používal jako anestetikum a v dnešní době byl nahrazen jinými bezpečnějšími látkami.
Přečtěte si také:Nitrosloučeniny — sloučeniny, které obsahují ve své molekule nitro (NO2) skupiny
Řešená cvičení na kyslíkové funkce
Otázka 1
(Uece) V organické chemii je funkční skupina definována jako molekulární struktura, která dává látkám podobné chemické chování. Množina sloučenin, které mají stejnou funkční skupinu, se nazývá organická funkce. Označte možnost, která správně prezentuje sloučeninu a organickou funkci, ke které patří.

Rozlišení:
Dopis C
Mezi alternativami je jediná, která správně vyjadřuje funkční skupinu k názvu chemické funkce, položka C. Organická esterová funkce je definována karbonylovou funkční skupinou, jejíž atom uhlíku má také kyslíkový ligand.
V položce A je vyjádřena etherová funkční skupina.
V položce B je vyjádřena ketonová funkční skupina.
V položce D je vyjádřena amidová funkční skupina. aminy to je amidy patří mezi dusíkové funkce.
otázka 2
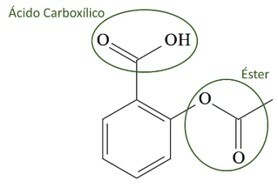
(UCS-RS) V 5. století př. Kr. C., Hippokrates, řecký lékař, napsal, že produkt z vrbové kůry zmírňuje bolest a snižuje horečku. Stejný produkt, kyselý prášek, je dokonce zmíněn v textech starověkých civilizací na Středním východě, v Sumeru, Egyptě a Asýrii. Domorodí Američané ho používali i proti bolestem hlavy, horečce, revmatismu a třesu. Tento lék je prekurzorem aspirinu, jehož chemická struktura je uvedena níže.
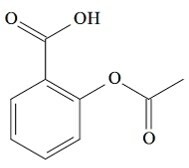
Organické funkce přítomné ve struktuře aspirinu, znázorněné výše, jsou:
a) karboxylová kyselina a ester.
b) alkohol a ether.
c) amin a amid.
d) amin a ether.
e) aminokyselina a alkohol.
Rozlišení:
Písmeno a
Autor: Ana Luiza Lorenzen Lima
Učitel chemie
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/funcoes-oxigenadas.htm
