A sublimace Jde o změnu fyzikálního stavu hmoty charakterizovanou přímým přechodem z pevné fáze do plynné fáze, aniž by procházela fází kapalnou. Přísně vzato, jakákoliv látka může podstoupit sublimaci, ale za určitých podmínek tlaku a teploty. Sublimace koreluje s tlakem par v pevné fázi, stejně jako s intermolekulárními interakcemi, které vyvíjejí pevné látky.
Tento proces lze snadno pozorovat na kousku suchého ledu, který se skládá z pevného oxidu uhličitého. Oxid uhličitý sublimuje pod tlakem a při pokojové teplotě. Opačný proces k sublimaci lze nazvat resublimací nebo depozicí. Aby došlo k sublimaci, musí hmota absorbovat energii, takže je považována za endotermický proces.
Přečtěte si také: Jaké jsou fyzikální stavy hmoty?
Shrnutí o sublimaci
Sublimace je přímý přechod z pevné fáze do plynné fáze, aniž by procházel fází kapalnou.
K pozorování sublimace látky jsou nutné specifické podmínky tlaku a teploty.
Sublimace je ovlivněna termodynamickými aspekty, jako je tlak par v pevné fázi a mezimolekulární interakce.
Sublimace je endotermický proces.
Příkladem sublimace je to, co se vyskytuje v suchém ledu, který se skládá z pevného oxidu uhličitého.
Co je sublimace?
sublimace je přímý přechod z pevné fáze do plynné fázebez průchodu kapalnou fází. Vyskytuje se za specifických podmínek teploty a tlaku pro některé pevné látky. Tento přechod je fyzikální proces změny stavu, který nezahrnuje chemické reakce.
Reverzní proces, tedy přímý přechod z plynné fáze do fáze pevné, se nazývá různě. Někteří autoři si pro tuto fázovou změnu ponechávají slovo sublimace, jiní používají „resublimace“ a dokonce „depozice“.
Jak funguje sublimace
Mezi sublimací a odpařováním lze nakreslit paralelu. V obou případech je konečným bodem plynná fáze. Rozdíl je samozřejmě ve výchozí fázi: pevná látka pro sublimaci a kapalina pro odpařování.
V obou případech, existuje vliv tlaku devapor a také termodynamické aspekty, zahrnující tepelné a mezimolekulární interakce.
Co je tlak par?
V uzavřené nádobě obsahující kapalinu je možné vnímat, že existuje rovnováha mezi kapalnou fází a parní fází. K tomu dochází, protože i pod teplotou varu je přítomná energie dostatečná k tomu, aby se některé molekuly kapaliny oddělily a přešly do páry. Některé molekuly par však mohou také znovu kondenzovat a vrátit se do kapalné fáze, což dokazuje reverzibilitu procesu.
Tato pára je vyrobena z hmota (má hmotnost a objem), cvičení tlak na povrch kapaliny, známý jako tlak páry. Nezáleží na množství kapaliny, ale na teplotě, protože čím vyšší je teplota, tím snáze se molekuly oddělují od kapalné fáze.
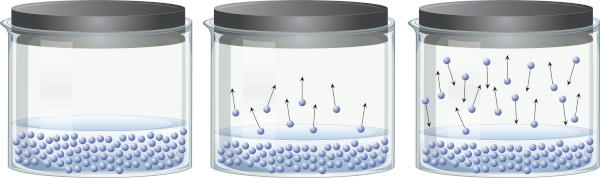
Kapaliny, které mají za běžných teplot vysoký tlak par, se nazývají těkavé. Například při 25 °C má ethylether tlak par 0,58 atm, aceton (propanon) má tlak par 0,29 atm, zatímco voda má tlak par 0,023 atm. Mimochodem, když je tlak par shodný s atmosférickým tlakem, kapalina vře. Chcete-li se dozvědět více o tlaku par, klikněte tady.
Tlak par a sublimace
I když v menší míře, pevné látky mají také tlak par, ale mnohem nižší než u kapalin. Například i při teplotě 1000 K je tlak par železa pouze 9,21 x 10-20 bankomat. Některé pevné látky však dokážou podstoupit sublimaci, jako je jód, což představuje vyšší tlak par za normálních teplot (4 x 10-4 bankomat).
To je možné pouze při přechodu molekul z pevného skupenství přímo do plynného skupenství. Aby se tak stalo, musí být přítomny molekuly pevné látky mezimolekulární interakce slabý (např. v jódu jsou typu indukovaného dipólu indukovaného dipólu).
Je to také vidět proces sublimace je endotermickýto znamená, že je potřeba, aby molekuly pevné látky absorbovaly energii ve formě tepla, aby mohly přerušit mezimolekulární interakce a přejít do stavu páry. Množství použitého tepla lze měřit termodynamickou veličinou známou jako entalpie sublimace.
Fázový diagram
Na vědět, v jakém rozsahu tlaku a teploty dojde k sublimaci pevné látky, musíte vyhodnotit svůj fázový diagram. Podívejme se na případ oxidu uhličitého, CO2.

Ve fázovém diagramu spojují hraniční čáry mezi stavy (pevná látka, kapalina a plyn) hodnoty tlaku a teploty pro dojde ke změně stavu. Při pozorování případu CO2 si všimneme, že při tlaku 1 atmosféry přechází pevná fáze přímo do plynné fáze při teplotě -78,5 °C, což charakterizuje sublimaci.
Oxid uhličitý má pouze kapalnou fázi při tlacích nad 5,11 atmosfér a nad tímto tlakem již není sublimace možná. Chcete-li se dozvědět více o fázovém diagramu, klikněte tady.
příklady sublimace
Suchý led: suchý led, často používaný k vytváření mlhových efektů na večírcích a akcích, je ve skutečnosti oxid uhličitý v pevném stavu.

naftalínové kuličky: naftalínové kuličky jsou vyrobeny z naftalenu, aromatické organické sloučeniny. Aplikuje se k odstranění nepříjemných pachů a také k odhánění molů, švábů a dalších jedovatých živočichů, proto se běžně používají ve skříních nebo dokonce pisoárech.

Kafr: S charakteristickým zápachem mohou sublimovat i oblázky kafru. Slouží také k odplašení komárů a prevenci plísní.

Jód: nekov patřící mezi halogeny také podléhá sublimaci.

Mezi předloženými látkami však pouze oxid uhličitý podléhá sublimaci za okolních podmínek. Ostatní, i se sublimací, mohou pod tlakem, ve kterém žijeme, podstoupit normální fúzi.
Přečtěte si také: Plazma — čtvrté skupenství hmoty
Vyřešená cvičení na sublimaci
Otázka 1
(Fuvest 2020) V supermarketech je běžné najít tzv. lyofilizované potraviny, jako je ovoce, zelenina a maso. Lyofilizované potraviny jsou i po delší době vhodné ke konzumaci i bez chlazení. Termín „lyofilizované“ v těchto potravinách označuje proces zmrazování a následnou dehydrataci sublimací vody. Aby došlo k sublimaci vody, je zapotřebí kombinace podmínek, jak ukazuje graf tlak-teplota, kde čáry představují fázové přechody.
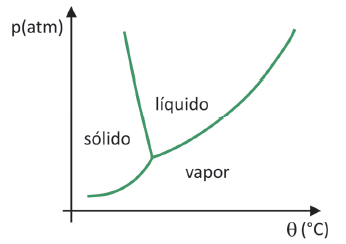
Přestože se jedná o proces, který průmyslově vyžaduje použití určité technologie, existují důkazy, že národy Předkolumbijští obyvatelé, kteří žili v nejvyšších oblastech And, dokázali potraviny zmrazit, takže je bylo možné skladovat více času. Zkontrolujte alternativu, která vysvětluje, jak došlo k přirozenému procesu lyofilizace:
a) Sublimace vody nastala v důsledku nízkých teplot a vysokého atmosférického tlaku v horách.
b) Potraviny byly po přirozeném zmrazení v chladných obdobích odvezeny do nejnižší části hor, kde byl nižší atmosférický tlak, což umožnilo sublimaci.
c) Potraviny byly vystaveny slunci, aby se zvýšila teplota, a nízký místní atmosférický tlak podporoval ztuhnutí.
d) Teploty byly v chladných obdobích dostatečně nízké na to, aby zmrazily potraviny, a nízký atmosférický tlak ve vysokých horách umožnil sublimaci.
e) Potraviny byly po přirozeném zmrazení stlačeny, aby se zvýšil tlak, aby mohlo dojít k sublimaci.
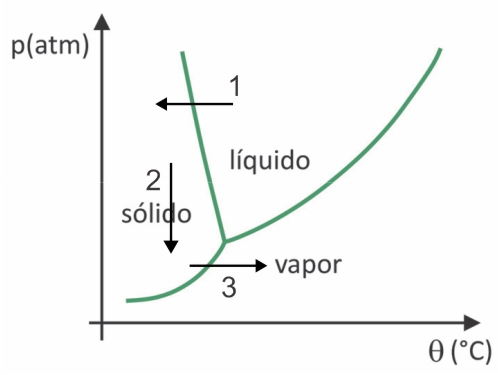
Odezva: Písmeno D.
Při lyofilizaci dochází k zamrzání vody s její následnou sublimací. Předkolumbovské národy mohly takový proces provést, protože v zimě mohla voda zamrznout (šipka 1) a při nízkém tlaku (šipka 2) v nejvyšších oblastech And by mohla podstoupit sublimaci (šipka 3).
otázka 2
(Uerj 2005) Suchý led nebo ztužený oxid uhličitý, široce používaný v chladicích procesech, podléhá sublimaci za okolních podmínek. Během této transformace dochází mimo jiné k jevům kolísání energie a narušení interakcí.
Tyto jevy jsou klasifikovány jako:
a) exotermické - interiontové
b) exotermická – mezijaderná
c) izotermické - meziatomové
d) endotermní - intermolekulární
Odezva: Písmeno D.
Sublimace je endotermický proces, protože vyžaduje absorpci tepla, aby se narušily interakce, které udržují molekuly pevné fáze kompaktní. Tyto interakce jsou intermolekulárního typu.
Autor: Stefano Araujo Novais
Učitel chemie

