Hlavním rozlišovacím znakem redoxních reakcí je, že jedna chemická látka současně ztrácí elektrony (oxidací) a druhá elektrony získává (redukcí).
U určitých reakcí je však možné pozorovat, že nedochází pouze k oxidaci a/nebo redukci. Níže je uveden příklad:
SnS + HCl + HNO3 → SnCl4 + S + NE + H2Ó
Výpočtem oxidačních čísel (Nox) všech atomů v této reakci, jak je uvedeno v textu „Stanovení oxidačního čísla (Nox)“, máme:
+2 -2 +1 -1 +1 +5 -2 +4 -1 0 +2 -2 +1 -2
SnS + HCl + HNO3 → SnCl4 + S + NE + H2Ó
Pojďme se nyní podívat, kterélátky trpěly změnami v jejich Nox a v důsledku toho oxidovaly a redukovaly:
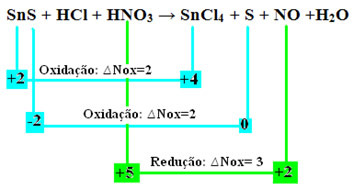
Všimněte si, že došlo ke dvěma oxidacím. Jak tedy v tom případě vyvážit chemickou rovnici?
Jedna důležitá věc, kterou je třeba mít na paměti, která platí pro všechny redoxní reakce, je ta počet odevzdaných elektronů se musí vždy rovnat počtu elektronů přijatých.
Proto, abyste vyvážili tento typ reakce, dodržujte stejná pravidla stanovená v textu "Redoxní vyvážení“, avšak s jedinou změnou: určení variace Nox (∆Nox) druhů, které generovaly dvě oxidace (SnS), bude součtem dvou ∆Nox, což nám dá celkovou hodnotu ztracených elektronů:
- SnS: ∆Total Nox = (∆Nox SnCl4) + (∆Nox S)
SnS: ∆Celkové NOx = 2 + 2 = 4
- HNO3: ∆Nox = 3
Pro vyvážení tedy můžeme pokračovat následujícími kroky:
Nepřestávej teď... Po reklamě je toho víc ;)
- SnS: ∆Celkové NOx = 4 → 4 bude koeficient HNO3;
- HNO3: ∆Nox = 3 → 3 bude koeficient SnS.
3 SnS + HCl + 4 HNO3 → SnCl4 + S + NE + H2Ó
Pokračování ve vyvažování zkušební metodou:
- Protože máte 3 Sn a 3 S v 1. členu, budou to také vaše koeficienty v 2. členu:
3 SnS + HCl + 4 HNO3 → 3 SnCl4 + 3 Y+NE+H2Ó
- S tím zůstal 2. člen 12 Cl (3. 4 = 12), takže 12 bude koeficient látky, ve které se Cl nachází v 1. členu, což je HCl:
3 SnS + 12 HCl + 4 HNO3 → 3 SnCl4 + 3 S + NO + H2Ó
- Nyní máme v 1. členu 16 H (12 + 4 = 16), odtud koeficient H2O se bude rovnat 8, protože 8 vynásobené vodíkovým indexem, který je 2, dává 16:
3 SnS + 12 HCl + 4 HNO3 → 3 SnCl4 + 3 S + NO +8H2Ó
- Dále v 1. členu jsou také 4 N, takže 4 bude také koeficient N ve 2. členu:
3 SnS + 12 HCl + 4 HNO3 → 3 SnCl4 + 3 S + 4 NO + 8 H2Ó
Všimněte si, že množství kyslíku v 1. končetině (3. 4 = 12) se rovná celkovému množství tohoto prvku ve 2. končetině (4 + 8 = 12). Reakce je tedy vyrovnaná.
Autor: Jennifer Fogaça
Vystudoval chemii
Chtěli byste odkazovat na tento text ve školní nebo akademické práci? Koukni se:
FOGAÇA, Jennifer Rocha Vargas. "Reakce s více než jednou oxidací a/nebo redukcí"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/reacoes-com-mais-uma-oxidacao-ou-reducao.htm. Zpřístupněno 27. července 2021.


