Miny jsou dusíkaté organické sloučeniny, které jsou odvozeny od látky amoniak (NH3) nahrazením jednoho nebo více vodíků organickými radikály. Podle množství substituovaných vodíků se aminy lze zařadit do:
Primární amin: vznikne nahrazením vodíku v amoniaku organickým radikálem;
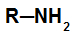
Obecná struktura primárního aminu
Sekundární amin: vzniklý nahrazením dvou vodíků amoniaku dvěma organickými radikály.

Obecná struktura sekundárního aminu
Terciární amin: vznikne nahrazením tří vodíků amoniaku třemi organickými radikály.

Obecná struktura terciárního aminu
Fyzikální vlastnosti aminů
Jsou to polární sloučeniny;
Primární a sekundární aminy jsou schopné fungovat Vodíkové vazby;
Terciární aminy provádějí interakci permanentní dipól;
Aminy s až pěti uhlíky jsou rozpustné ve vodě a ethanolu. Aminy se šesti nebo více uhlíky jsou prakticky nerozpustné ve vodě, ale rozpustné v organických rozpouštědlech;
Aminy, které mají aromatickou strukturu, jsou hustší než voda;
Aminy s jedním až třemi uhlíky jsou při pokojové teplotě plynné. Ti se čtyřmi až dvanácti uhlíky jsou kapalné při pokojové teplotě;
Obecně mají aminy vyšší teploty tání a teploty varu pouze ve vztahu k jakékoli nepolární organické sloučenině.
Chemické vlastnosti aminů
Jsou považovány za organické báze, podle Bronsted-Lowryho teorie;
Aromatické aminy mají nižší základní charakter kvůli jevu rezonance;
Čím větší je základní charakter aminu, tím je pravděpodobnější, že bude reagovat s určitou látkou;
V přítomnosti kyseliny se provádějí aminy neutralizační reakce, protože mají základní charakter.
pravidlo aminová nomenklatura
Chcete-li pojmenovat amin, jednoduše postupujte podle pravidla stanoveného Mezinárodní unií čisté a aplikované chemie (IUPAC), která je popsána níže:
Název radikálu nebo radikálů + amin
POZNÁMKA: Pokud má amin různé radikály, musíme postupovat podle abecedního pořadí.
Postupujte podle několika příkladů:
Příklad 1: primární amin

V primárním aminu v tomto příkladu máme přítomnost propylového radikálu, takže jeho název je propylamin.
Příklad 2: sekundární amin

V sekundárním aminu v tomto příkladu máme přítomnost methylového radikálu (nalevo od dusíku) a ethylového radikálu (napravo od dusíku). Jeho název je v abecedním pořadí ethyl-methylamin.
Příklad 3: terciární amin
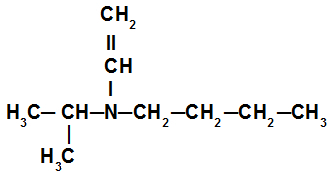
V sekundárním aminu v tomto příkladu máme isopropylový radikál (nalevo od dusíku), butylový radikál (napravo od dusíku) a vinylový radikál (pod dusíkem). Jmenuje se proto butyl-isopropyl-vinylamin.
Aminové aplikace
Široce se používá při výrobě různých organických sloučenin;
Používá se při výrobě mýdel;
Používá se v procesu vulkanizace gumy;
Používá se při výrobě barviv.
Podle mě. Diogo Lopes Dias
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-aminas.htm

