Dusíkaté funkce jsou jednou ze 4 funkčních skupin organických sloučenin. Sloučeniny, které patří do této funkce, jsou tvořeny dusíkem, proto se jim říká sloučeniny dusíku. Hlavními jsou aminy, amidy, nitrily a nitrosloučeniny.
Miny
Na aminy jsou organické sloučeniny, které lze nalézt v pevném, kapalném nebo plynném stavu. Jsou produkovány rozkladem zvířat a lze je nalézt také ve sloučeninách extrahovaných z rostlin.
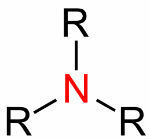
Obecný vzorec aminů
Jsou odvozeny od arylu nebo alkylu ve spojení s dusíkem. Aryl a alkyl nahrazují atomy vodíku. Podle této náhrady je lze klasifikovat takto:
- Primární: když je nahrazen pouze jeden vodík (R-NH2). Příklad: methanamin.
- Sekundární: když jsou nahrazeny dva vodíky (R.1R2NH). Příklad: dimethanamin.
- Terciární: když jsou nahrazeny tři vodíky (R.1R2R3N). Příklad: trimethanamin.
Aminy se používají při výrobě barviv, léků a mýdel.
Nomenklatura aminů je vytvořena následovně:
- nahrazení uhlovodíkové přípony „o“ slovem amin.
- označující polohu dusíku.
- označující typ vazby, en nebo in.
amidy
Na amidy jsou organické sloučeniny, které lze nalézt v pevném nebo kapalném stavu. Pocházejí z acylu vázaného na dusík a jsou vyráběny v laboratoři.
Molekulární vzorec amidů je CONH2, který je znázorněn takto:
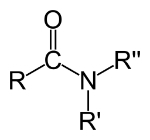
Obecný vzorec amidů
Amidy jsou klasifikovány podle počtu acylů vázaných na dusík, které mají:
- Primární: pokud má pouze jednu acylovou skupinu R-CO) NH2.
- Sekundární: pokud mají dvě acylové skupiny (R-CO) 2NH.
- Terciární: když mají tři acylové skupiny (R-CO) 3N.
Pokud jde o počet přítomných amidových skupin, je klasifikace následující:
Diamidy, pokud existují dvě skupiny amidů, a triamidy, pokud existují tři skupiny amidů atd.
Jeho aplikace v každodenním životě: mimo jiné výroba kosmetiky pro osobní péči (sprchový gel) a čisticích (čisticích) prostředků.
Název amidů je tvořen předponou, která udává počet uhlíků. Dále je přípona „oico“ pro uhlovodík nahrazena slovem amid.
Nitrosloučeniny
Nitrosloučeniny jsou organické sloučeniny nacházející se v kapalném stavu, které se nerozpouštějí ve vodě, protože jsou husté a vysoce reaktivní. Obecný vzorec pro nitrosloučeniny je NA2.
Aplikace nitrosloučenin je komplexní. Používají se jako výbušniny, jako rozpouštědlo a také při výrobě mastí a nástrojů.
Název nitrosloučenin vzniká spojením názvu hlavního řetězce se slovem nitro.
Nitrily
Nitrily, nazývané také kyanidy, jsou organické sloučeniny, které se nacházejí v pevném stavu a jsou rozpustné ve vodě. Obecný vzorec nitrilů je R - C ≡ N.
Tyto sloučeniny se používají při výrobě gumy, barviv, hnojiv a plastů.
Název nitrilů vzniká spojením názvu uhlovodíku se slovem nitril.
Přečtěte si také Okysličené funkce.
Cvičení
1. (Cesgranrio-RJ) Na začátku roku 1993 noviny uváděly, že když se člověk zamiluje, organismus syntetizuje látku - ethylfenylamin, zodpovědnou za její charakteristické buzení Stát.
Klasifikace a chemický charakter tohoto aminu jsou:
a) primární aminokyselina.
b) primární amin - bazický.
c) sekundární amin - neutrální.
d) sekundární aminokyselina.
e) sekundární amin - bazický.
Alternativa e: sekundární amin - bazický.
2. (UnB-DF) Acetoaminofen je látka, která má analgetické a antipyretické vlastnosti. Je uváděn na trh pod názvem Tylenol a jeho vzorec je uveden níže:
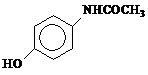
Zaškrtněte správné alternativy týkající se acetoaminofenu.
1. Patří do třídy fenolů;
2. Obsahuje také amidovou funkci;
3. Má vzorec C.8H9NA2;
4. Patří do třídy aromatických látek díky přítomnosti benzenového kruhu.
Všechny alternativy jsou správné



