Ó princip Le Chatelier nám říká, že když dojde k narušení systému v rovnováze, posune se směrem, který minimalizuje síly vytvořené tímto narušením a obnoví novou chemickou rovnováhu.
Jednou z těchto poruch je kolísání teploty. Tato variace je důležitá, protože kromě způsobení posunu rovnováhy změní také hodnotu rovnovážné konstanty KC.
Abychom lépe pochopili, jak k tomu dochází, podívejme se na příklad:
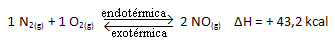
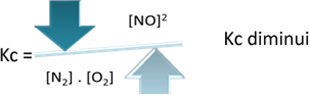
K.C = _[ NA]2___
[N2]. [Ó2]
Výše uvedená reakce probíhá v přímém směru s absorpcí energie, je endotermická. Na druhé straně k opačnému procesu dochází při uvolňování energie, což je exotermická reakce.
Pokud tedy zvýšíme teplotu systému, chemická rovnováha se posune směrem k endotermické reakci, která je v této reakci napravo. Je to tak, že teplo je absorbováno a rovnováha je znovu získána.
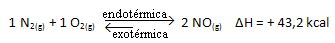
Opak je také pravdou; pokud snížíme teplotu tohoto systému, reakce se posune ve směru, kterým bude uvolňovat teplo, protože celková energie reakce se sníží. To znamená, že se rovnováha posune směrem k exotermické reakci, která je v tomto případě doleva:
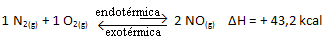
Ve zkratce:

Ve vztahu k rovnovážné konstantě (K.C), když se teplota zvýší, zvýhodňuje endotermickou reakci a více NO(G) vzniká, zvyšuje jeho koncentraci a snižuje koncentraci reaktantů. Ve vzorci níže si všimněte, že koncentrace NO(G) je přímo úměrná konstantě K.C, proto také zvyšuje:
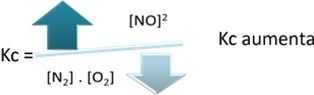
Pokud ale snížíme teplotu a posuneme reakci směrem k exotermní reakci, koncentrace NO produktu se sníží a koncentrace reaktantů se zvýší. Protože koncentrace reaktantů jsou nepřímo úměrné konstantě Kc, pak se sníží:
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/variacao-temperatura-deslocamento-equilibrio-quimico.htm
