K neutralizační reakci dochází, když kyselina reaguje s bází za vzniku vody a soli. Kyselina poskytuje H ionty+ a báze poskytuje OH ionty- pro tvorbu vody (H2Ó):
1 hodina+(tady) + 1 OH-(tady) → H2Ó(ℓ)
Tento typ reakce se nazývá „neutralizace“, protože pH média je neutralizováno; pH vody je 7,0 (neutrální).
Aby k těmto reakcím mohlo dojít, je nutné uvolnit určité množství tepla, které je pouze částí energie ionty se používají k vytváření vazeb, které vedou k molekulám vody, zatímco zbytek energie se uvolňuje do docela. Tato uvolněná energie se nazývá Neutralizační entalpie (∆Hneutralizace).

Jelikož uvolňuje teplo, odpovídá exotermickým reakcím, při nichž bude entalpie (globální energie systému) vždy záporná, menší než nula.
V případě reakce mezi silnými kyselinami a silnými zásadami bude hodnota neutralizační entalpie vždy rovna - 13,8 kcal / mol nebo - 57,7 kJ / mol. Stává se to proto, že zásady a silné kyseliny jsou v roztoku zcela disociované, a proto jediné Reakcí odpovědnou za projev tepla bude tvorba vody, jak je ukázáno ve třech níže uvedených příkladech:
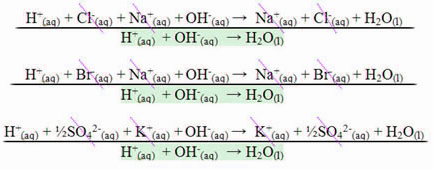
V případě neutralizačních reakcí zahrnujících slabé kyseliny nebo zásady bude hodnota neutralizační entalpie nižší než –57,7 kJ / mol.
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/quimica/entalpia-neutralizacao.htm
