Apolar je kvalita toho, co nemá polaritu, obvykle související s organickými molekulami.
V chemii polarita organických molekul souvisí s intenzitou elektronegativity atomů, které tyto molekuly tvoří. Pokud není rozdíl mezi elektronegativitou atomů, považuje se tato molekula za nepolární.
V nepolární molekule je rozdíl v elektronegativitě vazby atomů vždy musí být nula, protože ruší platnost.
Normálně jsou nepolární spojení tvořena Uhlovodíky, tj. Sloučeniny tvořené atomy uhlíku nebo vodíkem.
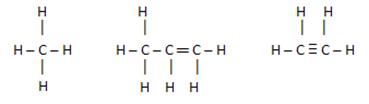
Tyto sloučeniny mají podobné elektronové náboje, takže mezi nimi nedochází k žádnému posunu náboje, ale zrušení těchto nábojů.
Viz také význam molekula.
Pokud jsou v uhlovodíkové vazbě například různé organické sloučeniny, je to již považováno za polární.
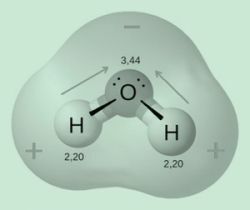 Příklad: molekulární geometrii vody (H2O) tvoří dva atomy vodíku a jeden z kyslíku že elektrony v této sloučenině jsou koncentrovanější v kyslíku, což způsobí posunutí zatížení. Kyslík se tedy stává elektronegativnějším než vodík, což charakterizuje tuto molekulu jako polární.
Příklad: molekulární geometrii vody (H2O) tvoří dva atomy vodíku a jeden z kyslíku že elektrony v této sloučenině jsou koncentrovanější v kyslíku, což způsobí posunutí zatížení. Kyslík se tedy stává elektronegativnějším než vodík, což charakterizuje tuto molekulu jako polární.
Jinými slovy, voda je polární sloučenina.
vědět více o Uhlovodíky.
nepolární a polární
Na rozdíl od nepolárních spojení polární molekuly jsou ty, které mají nenulovou elektronegativitu mezi atomy.
Kvůli různým hustotám elektronů hromadí některé atomy více elektronů než jiné, což zvyšuje přitažlivou sílu.
Některé z hlavních nepolárních sloučenin jsou: benzín, metan a etan.
Mezi hlavní polární sloučeniny patří: voda, cukr a alkohol.


