Izomerismus jedná se o přírodní jev, při kterém mají různé látky (z hlediska chemických a fyzikálních vlastností) přesně stejný molekulární vzorec, jako v následujícím příkladu:
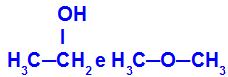
Různé látky, které mají stejný molekulární vzorec
Ethanol (vlevo) má molekulární vzorec C.2H6O, který se také vyskytuje u methoxyethanu (vpravo), jsou to tedy izomery.
Druhy izomerismu
→ plochý izomer
Jedná se o typ izomerismu, který studuje strukturální rozdíly mezi izomery.
The) obsazení
Jedná se o typ plochého izomerismu, ve kterém je rozdíl mezi látkami založen na rozdílu mezi organickými funkcemi, ke kterým patří. Podívejte se na několik příkladů:
Propanon a propan:
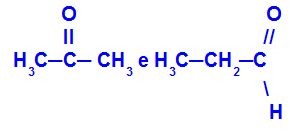
Izomery patřící k různým funkcím
Propanon (vlevo) patří do ketonové skupiny a propanal (vpravo) patří do aldehydové skupiny.
B) Vězení
Jedná se o typ plochého izomerismu, ve kterém je rozdíl mezi látkami založen na rozdílu mezi řetězci, které představují. Viz příklad:
2-methylpropan a butan
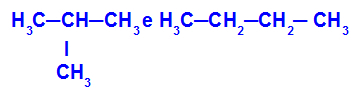
Izomery, které mají řetězce s různou klasifikací
V příkladu vidíme, že 2-methyl-propan (vlevo) má rozvětvený řetězec a butan (vpravo) má normální řetězec.
C) Pozice
Jedná se o typ plochého izomerismu, ve kterém je rozdíl mezi látkami založen na rozdílu v poloze složky přítomné v jejich řetězcích. Viz příklad:
1-chlorpropan a 2-chlorpropan
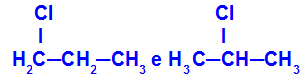
Izomery, které mají komponenty na různých pozicích v řetězci
V příkladu vidíme, že 1-chlorpropan (vlevo) má chlor umístěný na uhlíku 1 a 2-chlorpropan (vpravo) má chlor umístěný na uhlíku 2.
d) Metameria nebo kompenzace
POZNÁMKA: Izomerismus platný výlučně pro heterogenní řetězce.
Jedná se o typ plochého izomerismu, ve kterém je rozdíl mezi látkami založen na rozdílu v poloze heteroatomu přítomného v jejich řetězcích. Viz příklad:
Příklad: Methoxypropan a ethoxyethan
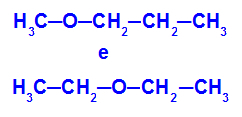
Izomery, které mají heteroatomy na různých pozicích v řetězci
V příkladu vidíme, že v methoxypropanu (vlevo) má kyslík radikál s jedním uhlíkem na jedné straně a třemi uhlíky na druhé straně. V ethoxyethanu (vpravo) má kyslík radikál se dvěma uhlíky na jedné straně a dvěma uhlíky na druhé straně.
a)Tautomery
Jedná se o konkrétní případ izomerismu rovinné funkce a vyskytuje se pouze ve třech organických funkcích:
Aldehyd
keton
Enol
Tento typ izomerismu funguje na skutečnosti, že existuje chemická rovnováha mezi enolem a aldehydem a mezi enolem a ketonem, to znamená, že tyto složky se na sebe neustále převádějí. Viz příklad:
Prop-2-en-1-ol a propanon
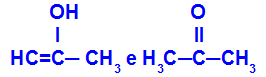
Izomery patřící k různým funkcím
V příkladu vidíme, že Prop-2-en-1-ol (vlevo) patří do skupiny enolů a propanon (vpravo) patří do skupiny ketonů, takže jsou izomery tautomery.
→ Izomerismus vesmíru
Jedná se o typ izomerismu definovaný prostorovou analýzou molekuly.
a) Geometrické izomery
Nepřestávejte... Po reklamě je toho víc;)
Jedná se o typ prostorového izomerismu, ke kterému dochází, když má látka molekuly s následujícími vlastnostmi:
Uzavřený řetězec, který má dva uhlíky se dvěma různými ligandy, jako v příkladu níže:

Uzavřená struktura s geometrickým izomerismem
Otevřený řetězec, který má dvojnou vazbu mezi uhlíky a v každém z těchto uhlíků dvojné vazby existují dva různé ligandy, jako v příkladu níže:
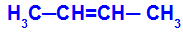
Otevřená struktura s geometrickým izomerismem
Geometrický izomerismus je rozdělen do dvou skupin:
1Ó Skupina: cis-trans
Nastává, když jsou dva ligandy jednoho uhlíku striktně stejné jako dva ligandy druhého uhlíku, ať už v otevřené struktuře nebo v uzavřené struktuře.
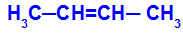
Řetězec látky, která má cis-trans izomerismus
Izomer se bude nazývat cis, když jsou stejné ligandy ve stejné rovině.

Příklad cis izomeru
Izomer bude nazýván trans, když jsou různé ligandy ve stejné rovině.

Příklad trans izomeru
2Ó Skupina: E-Z
Nastává, když jsou dva ligandy jednoho uhlíku odlišné ve vztahu ke dvěma ligandům druhého uhlíku, ať už v otevřené struktuře nebo v uzavřené struktuře.

Řetězec látky, která má izomerismus E-Z
Izomer se bude nazývat E, když jsou ligandy s nejvyšším atomovým číslem v opačných rovinách. V níže uvedeném příkladu má uhlík nalevo Br s nejvyšším atomovým číslem (35) a na druhém je kyslík (8).
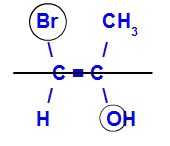
Příklad E-izomeru
Izomeru se bude říkat Z, když budou ligandy s nejvyšším atomovým číslem ve stejné rovině. V níže uvedeném příkladu má uhlík nalevo Br s nejvyšším atomovým číslem (35) a na druhém je kyslík (8).

Příklad Z-izomeru
B) optický izomer
Jedná se o typ prostorového izomerismu, ke kterému dochází, pouze pokud má látka molekuly chirální uhlík (ten, který má čtyři různé ligandy) ve svých strukturách. Molekula s chirálním uhlíkem má schopnost polarizovat a vychylovat světlo následovně:
Vpravo (pravý izomer)
Vlevo (levotočivý izomer)
Sloučenina s optickou aktivitou vždy měla aktivní izomery (nazývané optické antipody) a neaktivní izomery (směs mezi dvěma aktivními izomery, směs zvaná racemická).
Pomocí následujícího vzorce můžeme určit počet aktivních (IOA) a neaktivních (IOI) izomerů sloučeniny, která má chirální uhlík:
IOA = 2Ne
IOI = 2Ne
2
Níže je uveden příklad sloučeniny, která má geometrický izomerismus:
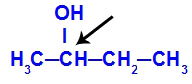
Chirální uhlík obsažený v butan-2-olu
Struktura butan-2-olu má následující ligandy:
Methyl (CH3)
Ethyl (CH3-CH2)
Vodík (H)
Hydroxyl (OH)
Protože má pouze jeden chirální uhlík, má tedy butan-2-ol:
Aktivní izomery:
IOA = 21
IOA = 2
Neaktivní izomery:
IOI = 21
2
IOI = 2
2
IOI = 1
Podle mě. Diogo Lopes Dias
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
DNY, Diogo Lopes. „Co je to izomerismus?“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria.htm. Zpřístupněno 27. června 2021.
