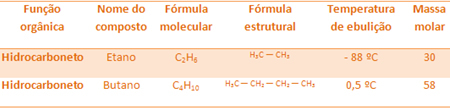
Jeden substituční reakce je založen na výměně mezi složkami dvou různých reagencií. Sloučeniny s větší stabilitou (nasycené, tj. Pouze s jednoduchými vazbami mezi uhlíky) tento proces podstoupí s větší pravděpodobností. Benzen to však také dokáže.
Víme to ve struktuře benzen existují tři dvojné vazby (tři vazby pí), to znamená, že tato sloučenina je nenasycená, ale tyto dvojníky podléhají fenoménu rezonance (střídání polohy tří vazeb pí) po celou dobu. Z tohoto důvodu má jeho struktura větší stabilitu, protože vazby procházejí všemi uhlíky.
Substituční reakce, které mohou nastat v benzenu, jsou:
Halogenace;
Nitrace;
Sulfonace;
Alkylace;
Acylace.
a) Halogenace
Při této reakci benzen interaguje s halogeny (Br2, Cl2 Ahoj2), vždy za přítomnosti katalyzátoru, kterým může být anorganická sůl (AlCl3, FeCl3 a FeBr3). Proces probíhá výměnou benzenového vodíku za atom halogenu. Výsledkem je tvorba organického halogenidu a halogenovaný hydrid. Viz příklad:
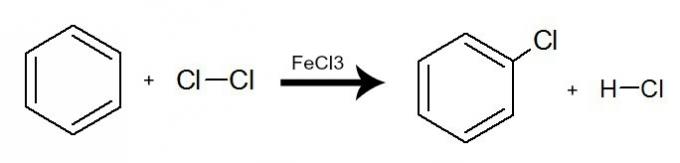
Rovnice představující halogenaci benzenu za použití molekulárního chloru (Cl2)
b) Nitrace
Při této reakci benzen interaguje s kyselinou dusičnou (HNO3), vždy za přítomnosti katalyzátoru na bázi kyseliny sírové (H2POUZE4) a topení. Proces probíhá výměnou vodíku z benzenu za skupinu NO2 kyseliny. Výsledkem je vznik a nitrosloučenina a voda.
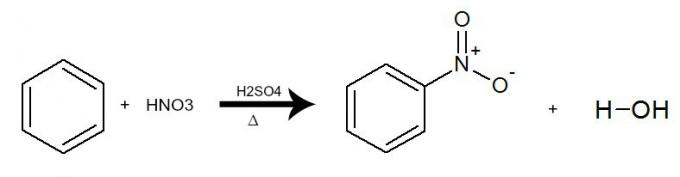
Rovnice představující nitraci benzenu za použití kyseliny dusičné
c) Sulfonace
V této reakci benzen interaguje s kyselinou sírovou (H2POUZE4), vždy za přítomnosti katalyzátoru na bázi oxidu sírového (SO3) a topení. Proces probíhá výměnou vodíku z benzenu skupinou SO3H kyseliny. Výsledkem je vznik kyselina sulfonický a voda.
Nepřestávejte... Po reklamě je toho víc;)
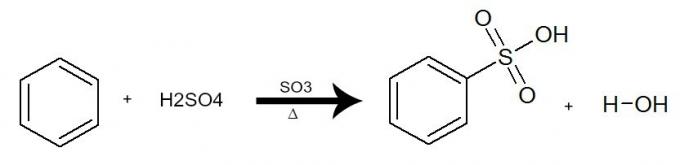
Rovnice představující sulfonaci benzenu za použití kyseliny sírové
d) Alkylace
V této reakci benzen interaguje s a organický halogenid (R-X), vždy s přítomností katalyzátor chlorid hlinitý (AlCl3) a topení. Proces probíhá výměnou vodíku z benzenu skupinou R (organický substituent) z halogenidu. Výsledkem je tvorba rozvětveného aromatického uhlovodíkua anorganickou kyselinu (HX).
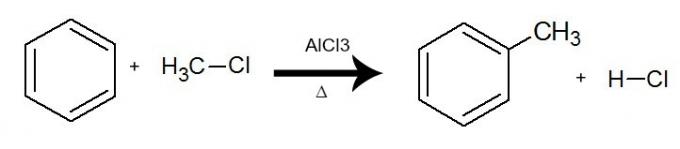
Rovnice představující alkylaci benzenu za použití chlormethanu
e) Acylace
V této reakci benzen interaguje s halogenidem kyseliny, který může být reprezentován ethanoylchloridem:
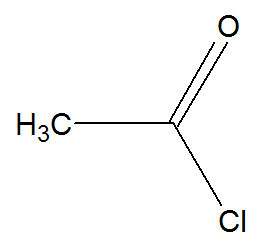
Strukturní vzorec ethanoylchloridu
Reakce probíhá za přítomnosti katalyzátor chlorid hlinitý (AlCl3) a dochází k výměně jednoho vodíku z benzenu za celou halogenidovou skupinu (s výjimkou X-halogenu). Výsledkem je vznik a keton a anorganická kyselina (HX). Viz příklad:
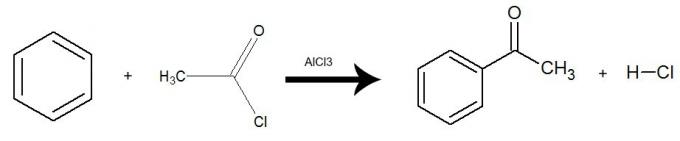
Rovnice představující acylaci benzenu za použití ethanoylchloridu
Podle mě. Diogo Lopes Dias
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
DNY, Diogo Lopes. "Substituční reakce v benzenu"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/reacoes-substituicao-no-benzeno.htm. Zpřístupněno 27. června 2021.
Chemie

Aromatické sloučeniny, areny, polarita, nerozpustný, rozpustný, nepolární rozpouštědla, ether, tetrachlormethan, uhlovodíky, insekticidy, barviva, rozpouštědla, výbušniny, karcinogeny, toluen, methylbenzen, léky, lepidlo švec.
Chemie

Klikněte sem a dozvíte se více o substituční reakci, chemickém procesu, při kterém si použitá činidla (organická a anorganická) vyměňují jednu ze svých složek navzájem a vytvářejí nové látky. Mezi látky, které se nejčastěji používají jako činidla, patří alkany, benzen a organické halogenidy.