Atomové číslo, symbolizované písmenem Z, odpovídá množství protonů existujících v jádru atomu daného chemického prvku. Například atomové číslo vodíku je 1, což znamená, že má v atomovém jádře pouze 1 proton.
Atomové číslo se obvykle objevuje vedle symbolu dolního indexu chemického prvku (v dolním rohu) vlevo. Příklad: 1H.
V základním stavu se atomové číslo rovná počtu elektronů, protože v tomto stavu je prvek neutrální, proto se množství kladných nábojů (protonů) musí rovnat množství záporných nábojů (elektronů) atom.
Atomové číslo je důležité, protože je to on, kdo určuje hlavní charakteristiky a vlastnosti prvku, stejně jako jeho chování a umístění v periodické tabulce. Prvky jsou uvedeny v periodické tabulce ve vzestupném pořadí podle atomového čísla, které se obvykle objevuje nad prvkem, jak je znázorněno níže. Všimněte si, že prvním prvkem je vodík, H (Z = 1), následovaný heliem, He (Z = 2), poté přijde lithium, Li (Z = 3) atd.
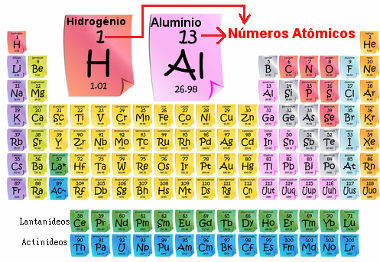
Atomový počet prvků v periodické tabulce
Můžeme dokonce konceptualizovat chemický prvek jako bytí
„Sada atomů, které mají stejné atomové číslo“. Když tedy mluvíme například o chemickém prvku kyslík, mluvíme o atomech s atomovým číslem 8. Níže máme atomy chemických prvků z období 1 a 2 periodické tabulky ve vzestupném pořadí podle atomového čísla:
Chemické prvky z období 1 a 2 periodické tabulky ve vzestupném pořadí podle atomového čísla
Atomová čísla původně definoval anglický fyzik Henry Gwyn Jeffreys Moseley (1887-1915) a při provádění experimentů zahrnujících bombardování různých prvků chemici s rentgenovými paprsky, zjistil, že druhá odmocnina frekvence rentgenových paprsků produkovaných emisí atomového jádra byla přímo úměrná atomovému číslu prvku v tabulce. Periodické. S tím dospěl k závěru, že atomové číslo souviselo s vlastnostmi atomů, protože představovalo počet kladných nábojů v jádru každého atomu.
Chemické vazby neovlivňují atomový počet atomů, protože zahrnují pouze elektrony, které jsou v elektrosféře. Jaderné reakce však zahrnují atomové jádro, a proto je zahrnuto také atomové číslo.
Například když jsou částice (hlavně umírněné neutrony) bombardovány na těžké nestabilní atomové jádro, toto jádro je rozbité a vznikají dvě menší atomová jádra, tj. s menším počtem protonů a neutronů, uvolňující kolosální množství energie.
Jaderná fúze je naproti tomu opačný proces, kdy se spojují dvě malá a lehká jádra, která vytvářejí větší a stabilnější jádro a uvolňují ještě větší množství energie.
Kdykoli tedy dojde k těmto jaderným reakcím, vznikají nové chemické prvky, protože atomová čísla počátečních prvků se liší od atomových čísel konečných prvků. Například viz níže, že štěpení uranu-235 s atomovým číslem 92 vede k baryu (Z = 56), kryptonu (Z = 36) a třem neutronům:

Reakce štěpení uranu-235
Autor: Jennifer Fogaça
Vystudoval chemii
Zdroj: Brazilská škola - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-numero-atomico.htm

