THE aktivační energie je to minimální množství energie potřebné k tomu, aby došlo ke kolizi mezi částicemi reaktantu ve výhodné orientaci, která má za následek reakci.
K reakcím dochází pouze v případě, že reaktanty mají aktivační energii (nebo minimální potřebnou energii, která se liší od reakce k reakci; buď v množství nebo formě) nebo pokud jim je dodán.
Například při kontaktu kovového sodíku s vodou reaguje prudce. To znamená, že energetický obsah těchto reaktantů je již dostatečný pro uskutečnění reakce.
V případě zapnutí kamen dojde ke spalovací reakci pouze tehdy, když v blízkosti plynu, který se kamny uvolňuje, umístíme zapálenou zápalku nebo jiný zdroj ohně. To znamená, že v tomto případě bylo nutné dodávat energii do systému tak, aby dosáhl aktivační energie a reakce proběhla.
V případě samotného použitého fosforu je pro jeho spalování aktivační energie zajištěna třením. Totéž se děje se zapalovači, které také potřebují jiskru, která dodává potřebnou aktivační energii pro spalování plynu v nich obsaženého.
Aktivační energii lze zajistit také světlem, jako je tomu v případě rozkladu peroxidu vodíku. Proto je uložen v tmavých nebo neprůhledných lahvích.
Nepřestávejte... Po reklamě je toho víc;)

Můžeme tedy dojít k závěru, že aktivační energie (E.dokud) je rozdíl mezi energií potřebnou k zahájení reakce (E) a energií obsaženou v reaktantech (Epr):

Aktivační energie je překážkou pro uskutečnění reakce a je zapotřebí k rozbití vazeb reaktantů. Díky tomu probíhá reakce a vytvářejí se nová spojení za účelem vytvoření produktů.
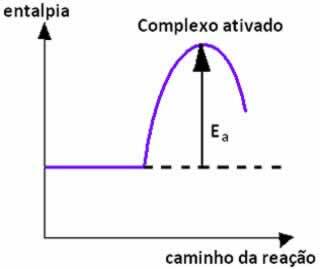
Když ke srážce mezi částicemi reaktantů s příznivou orientací dojde se stejnou energií nebo vyšší než aktivační energie, před vznikem produktů se vytvoří střední a nestabilní stav, denominováno aktivovaný komplex, ve kterém jsou vazby reaktantů oslabeny a vytvářejí se vazby produktů. Tím pádem, aktivační energie je energie potřebná k vytvoření aktivovaného komplexu.
Níže máme graf, který ukazuje aktivační energii jako bariéru pro uskutečnění reakce:
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. "Aktivační energie"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/energia-ativacao.htm. Zpřístupněno 27. června 2021.