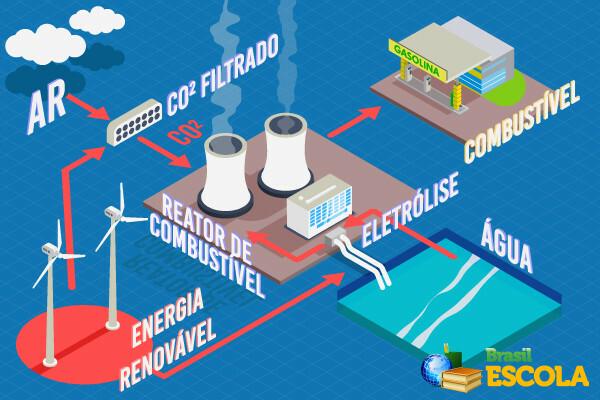
Atomy jsou nekonečně malé částice, které tvoří veškerou hmotu ve vesmíru. V průběhu času se představa o tom, jak by vypadala atomová struktura, změnila podle nových objevů vědců. Více se o tom dozvíte v textuVývoj atomového modelu.
Model je reprezentací reality (nikoli samotné reality), takže atomové modely jsou reprezentacemi hlavní složky atomu a jeho strukturu a vysvětlit určité fyzikální a chemické chování hmoty. To se děje proto, že pro lidskou bytost ještě není možné vidět izolovaný atom ani při použití ultramikroskopů.
Chcete-li získat představu o tom, jak malý je atom, vězte to The Nejmenší částice viditelná pod běžným mikroskopem obsahuje přes deset miliard atomů! Atom je tak malý, že, kdybychom je položili vedle sebe milion, nedosáhli bychom tloušťka vlasů.
Myšlenková mapa: Atom
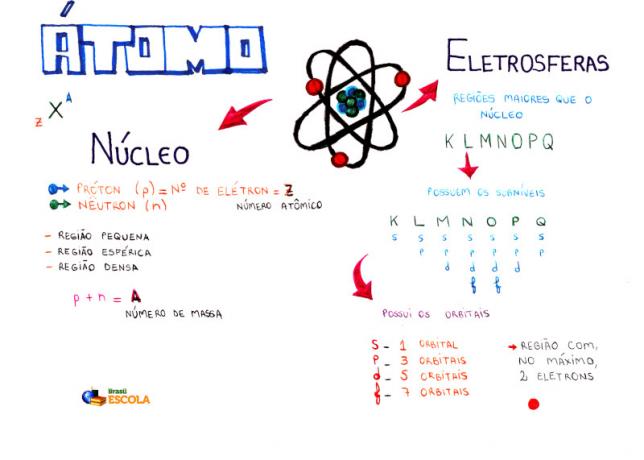
* Chcete-li stáhnout myšlenkovou mapu v PDF, Klikněte zde!
Z atomových modelů je v současné době na střední škole nejpoužívanějším modelem pro pochopení struktury atomu a jeho vlastností Rutherford-Bohrův model. Podle tohoto modelu se struktura atomu skládá ze dvou hlavních částí: jádro a elektrosféra.

Dvě hlavní části struktury atomu - elektrosféra a jádro
* Jádro: Představuje centrální část atomu, je kompaktní, masivní a velmi hustý, navíc je tvořen částicemi o větší hmotnosti, kterými jsou protony a neutrony.

Ilustrace protonů a neutronů, které tvoří atomové jádro
- Protony: jsou to částice s kladným elektrickým nábojem (relativní náboj = +1; poplatek v coulombu (C) = +1,602. 10-19) a jeho relativní hmotnost se rovná 1.
Skutečnost, že protony tvoří jádro a dodávají mu celkový kladný náboj, objevila Eugen Goldstein, v roce 1886 úpravou Crookesovy ampule a několika experimenty. Viděl, že při velmi vysokém napětí se objevují emise (anodové paprsky - zbytky atomů plynu, které byly uvnitř žárovky a jejichž elektrony byly vytrženy elektrickým výbojem). Umístěním elektrického nebo magnetického pole mimo žárovku se tyto paprsky odklonily směrem k zápornému pólu. To znamenalo, že existovaly pozitivní subatomární částice, které se nazývaly protony.
Později, Ernest Rutherford (1871-1937) provedl experiment popsaný v textu Rutherfordův atom, což ho vedlo k objevení polohy protonu: v jádře.
- Neutrony: jsou to částice s hmotností rovnou hmotnosti protonů (1), ale jak název napovídá, jsou neutrální, to znamená, že nemají elektrický náboj.
Neutrony byly objeveny v roce 1932 James Chadwick (1891-1974), který si uvědomil, že jádro radioaktivního berýlia emitovalo neutrální částice s hmotností zhruba rovnou hmotnosti protonů (ve skutečnosti je o něco větší).
Nepřestávejte... Po reklamě je toho víc;)
Průměr jádra závisí na množství protonů a neutronů, které atom má, ale v průměru se pohybuje kolem 10-14 měsíc 10-15 m.
Atomové jádro koncentruje prakticky celou hmotnost atomu, což je velmi malá část: proton i neutron jsou asi 100 000krát menší než celý atom samotný! Pro srovnání si představte, že zvětšíme jádro atomu prvku vodík (který má pouze proton) o velikosti tenisového míčku, nejbližší elektron by byl asi tři kilometry od vzdálenost! I kdyby byl atom zvětšen do výšky 14patrové budovy, jeho jádro by mělo velikost pouhého zrnka soli v sedmém patře. Je to opravdu něco úžasného, nemyslíte ?!
* Elektrosféra: Je oblast, kde se elektrony otáčejí kolem jádra. Přestože je to oblast mnohem většího objemu než jádro, je prakticky prázdná, protože každý elektron je 1836krát menší než 1 proton (nebo než 1 neutron). Proto je hmotnost atomu prakticky celá v jádru. Elektrony jsou částice se záporným elektrickým nábojem (-1).
Elektrony byly objeveny v roce 1897 Joseph John Thomson (1856-1940), tvůrce Thomsonův atomový model. Thomsonův experiment lze podrobně vidět v textu Thomsonův experiment s elektrickými výboji, ale ve zkratce použil výše zmíněnou ampulku Crookes a uvědomil si, že katodové paprsky byly vždy přitahován kladným pólem, který dokázal, že atom měl záporné částice, které byly vyvolány elektrony.
Elektrony se otáčejí kolem jádra miliardkrát za miliontinu sekundy, formují atom a nechávají ho chovat se, jako by byl pevný.
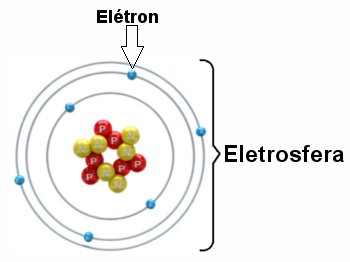
Ilustrace elektrosféry se třemi elektronovými vrstvami a elektrony rotujícími kolem jádra.
Stručně řečeno, můžeme vytvořit tabulku pro rozlišení tří hlavních subatomárních částic, které jsou součástí struktury atomu:

Hmotnostní a elektrický náboj tří hlavních subatomárních částic - protonů, neutronů a elektronů
Atomy všech chemických prvků se skládají z těchto tří subatomárních částic. To, co se liší od jednoho chemického prvku od druhého, je množství, ve kterém se tyto částice objevují, zejména množství protonů v jádru, které se říká atomové číslo. Pokračujte ve studiu prostřednictvím textu. Chemický prvek.
* Mind Map by Me. Diogo Lopes
Autor: Jennifer Fogaça
Vystudoval chemii
Chemie
Klasifikace látek, vody, kyanovodíku, oxidu uhličitého, amoniaku, vodíku, helia, látek jednoduché, složené látky, směsi, fáze směsi, homogenní směs, směs heterogenní.