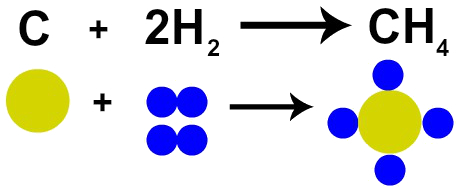
Jak aldehydy, tak ketony mají jako funkční skupinu karbonyl. Rozdíl je v poloze tohoto karbonylu. Jak je uvedeno níže, v aldehydech se karbonyl jeví jako navázaný na vodík, to znamená, že vždy přijde na konci. Na druhou stranu, v ketonech je karbonylová skupina mezi dvěma uhlíky, nikdy nepřichází na konec uhlíkových řetězců:
Aldehydy: Ketony:
ÓÓ
║║
H ─ C ─ C ─ C ─C
Hlavní způsoby získání sloučenin patřících do těchto skupin jsou: hydratace alkynů, ozonolýza alkenů a oxidace alkoholů. V případě ketonů stále existuje speciální metoda, kterou je tepelný rozklad organických vápenatých solí.
Podívejte se, jak každý z těchto procesů funguje:
1. Alkynes Hydration:K přidání molekul vody v kyselém prostředí dochází v přítomnosti katalyzátoru HgSO4.
Zpočátku se vytvoří meziproduktová sloučenina, enol, který se transformuje na aldehyd.
Pokud je alkynem, který reaguje, ethyn, dojde k tvorbě aldehyd-ethanalu. Pokud ale jde o jakýkoli jiný alkyn, vytvoří se odpovídající ketony následovně Markovnikovovo pravidlo
, kde se vodík ve vodě přidá k uhlíku v trojné vazbě, která má k sobě připojeno nejvíce vodíků: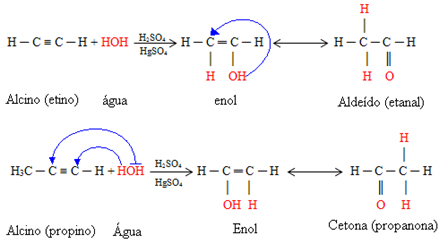
2. Ozonolýza alkenů: Ozon (O.3) se přidá k dvojné vazbě alkenu v oxidační reakci za přítomnosti vody a zinku.
Nepřestávejte... Po reklamě je toho víc;)
Nejprve se vytvoří meziprodukt, ozon, který hydrolyzuje na odpovídající aldehyd a keton.
Níže je ozonolýza 2-methyl-prop-1-enu, za vzniku propan-2-onu a methanolu:
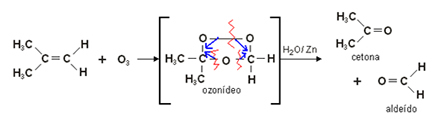
3. Oxidace alkoholů: Alkoholy mohou podléhat oxidaci, když jsou vystaveny oxidačnímu činidlu, jako je vodný roztok dichromanu draselného (K.2Cr2Ó7) nebo manganistan draselný (KMnO4) v kyselém prostředí.
Pokud je alkohol primární, vzniká částečnou oxidací aldehyd. Ale pokud se jedná o celkovou oxidaci, aldehyd se změní na karboxylovou kyselinu. Pokud se chceme zastavit na aldehydu, jednoduše proveďte tento proces při teplotě vyšší, než je teplota varu vzniklého aldehydu. Tímto způsobem se odpařuje a destiluje prostřednictvím specifického přístroje.

Pokud je alkohol sekundární, produktem jeho oxidace bude keton.
Příklad:
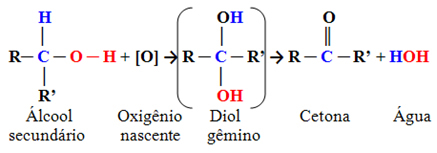
Terciární alkoholy nepodléhají oxidaci.
4. Specifická metoda pro získání ketonů: Zahřívání vápenatých solí karboxylové kyseliny. Tyto soli podléhají rozkladu a kromě ketonu vznikají uhličitan vápenatý:
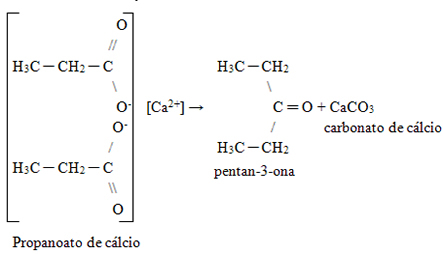
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. "Metody získávání aldehydů a ketonů"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/metodos-obtencao-aldeidos-cetonas.htm. Zpřístupněno 28. června 2021.
Chemie

Aldehydy, karbonylové sloučeniny, karbonylová skupina, hlavní aldehydy, Ethanal, surovina v pesticidním a farmaceutickém průmyslu, Metanal, formaldehyd, plasty a pryskyřice.
Chemie

Ketony, organické látky, karbonylová funkční skupina, získání rozpouštědla skloviny, propanon, ketolátky v krvi, extrakce olejů a tuků ze semen rostlin, rozpouštědla Organické.