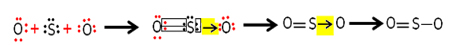
Když smícháme kyselinu chlorovodíkovou (HCℓ) a hydroxid sodný (NaOH), dojde k neutralizační reakci, kterou lze vyjádřit následující chemickou rovnicí:
HCℓ(tady) + NaOH(tady) → NaCℓ(tady) + H2Ó(ℓ)
Tato reakce zahrnuje chemické látky ionizované ve vodném prostředí. Dotyčná kyselina uvolňovala ionty H ve vodném roztoku+(tady) a Cℓ-(tady)a báze uvolnila ionty Na+(tady) a oh-(tady). Tyto ionty reagovaly a vytvořily rozpustnou sůl (chlorid sodný) a vodu.
Tuto reakci pak můžeme vyjádřit iontovou rovnicí:
H+(tady) + Cℓ-(tady) + Dovnitř+(tady) + OH-(tady) → NaCℓ(tady) + H2Ó(ℓ)
nebo
H+(tady) + Cℓ-(tady) + Dovnitř+(tady) + OH-(tady) → V+(tady) + Cℓ-(tady) + H2Ó(ℓ)
Tím pádem, iontová rovnice je chemická rovnice, ve které se objevují ionty i atomy a molekuly.
Můžeme také napsat iontovou rovnici v menší formě. Například v reakci, kterou uvažujeme, ionty Na+(tady) a Cℓ-(tady) se nazývají divácké ionty, a proto je lze v redukované iontové rovnici ignorovat:
Nepřestávejte... Po reklamě je toho víc;)
H+(tady) + OH-(tady) → H2Ó(ℓ)
Tento typ rovnice umožňuje lépe vizualizovat neutralizaci, ke které v systému došlo.
Mnoho iontových reakcí zahrnuje tvorbu nerozpustných solí, tj vyrážka. Například když smícháme dva vodné roztoky dusičnanu olovnatého a jodidu sodného, jsou v médiu ionty, které navzájem reagují a tvoří vysrážený jodid olovnatý (žlutá pevná látka).

Chemická rovnice pro tuto reakci je dána vztahem:
Pb (č3)2 (aq) + 2 NaI(tady) → PbI2 (s) + 2 NaNO3 (aq)
Iontovou rovnici a redukovanou iontovou rovnici lze reprezentovat následovně:
Pb2+(tady) + 2 NE3-(tady) + 2 palce+(tady) + 2 já-(tady) → PbI2 (s) + 2 palce+(tady) + 2 NE3-(tady)
Pb2+(tady) 2 já-(tady) → PbI2 (s)
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. "Iontové rovnice"; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/equacoes-ionicas.htm. Zpřístupněno 28. června 2021.
Funkce chemické rovnice, způsob popisu chemické reakce, činidla, produkty, Katalyzátory, sraženina, reverzibilní reakce, stechiometrický koeficient, různé podíly látky.