THE řetězová izomerie je typ plochého nebo konstitučního izomerismu, tj. ve kterém dvě nebo více sloučenin mají stejné molekulární vzorec (stejné chemické prvky a ve stejném množství), ale liší se podle vzorce strukturální.
V případě izomerismu řetězce (nazývaného také izomerismus jádra nebo skeletální izomerismus) patří sloučeniny ke stejné organické funkci, ale rozdíl je v typu řetězce.
Například můžeme mít následující případy:
1 - Jeden izomer může mít otevřený (acyklický) řetězec, zatímco druhý má uzavřený (cyklický) řetězec;
2 - Jeden izomer může mít řetězec nasycený (pouze jednoduché vazby mezi uhlíky), zatímco druhý izomer je nenasycený (má alespoň jednu dvojnou vazbu mezi uhlíky);
3 - Jeden má normální řetězec, zatímco druhý má rozvětvený řetězec;
4 - Jeden má homogenní řetězec a druhý má heterogenní řetězec.
Máte-li jakékoli dotazy týkající se těchto typů uhlíkových řetězců, přečtěte si text Klasifikace uhlíkových řetězců.
Nyní se podívejme na několik příkladů izomerismu řetězce:
1- Otevřený a uzavřený řetězec:
Následující izomery mají molekulární vzorec C5H10, ale liší se tím, že jeden má otevřený řetězec a druhý má uzavřený řetězec:

Řetězové izomery (otevřené a uzavřené)
Tento příklad navíc zapadá do následujícího typu izomerismu řetězce:
2 - Nasycený a nenasycený řetězec:
V předchozím příkladu jsme viděli, že řetězec pent-1-en je nenasycený, protože má dvojnou vazbu mezi dvěma uhlíky, zatímco cyklopentan je nasycený, to znamená, že má pouze jednoduché vazby.
Viz další příklad: Molekulární vzorec: C3H6:
CH2 ═ CH ─ CH3 a CH2
/ \
H2C CH2
propencyklopropan
Nepřestávejte... Po reklamě je toho víc;)
3- Normální a rozvětvený řetězec:
Tento typ izomerismu se může vyskytovat v uzavřených nebo otevřených řetězcích. Například cyklopentan zobrazený v první položce nemá žádné větve, ale další z jeho izomerů, methylcyklobutan, ano. Dívej se:

Řetězové izomery (normální a rozvětvené)
Nyní se podívejme na příklad tohoto typu izomerismu s otevřeným řetězcem. Molekulární vzorec následujících izomerů je: C4H8Ó2:
H3C CH2 ─ CH2─ COOH a CH3 ─ CH ─ COOH
│
CH3
Kyselina butanová Kyselina 2-methylpropanová
4- Homogenní a heterogenní řetězec:
Homogenní řetězec je takový, který má pouze atomy uhlíku, zatímco heterogenní řetězec je ten, který má a heteroatom, tj. atom nějakého chemického prvku mezi uhlíky, jako je kyslík, dusík, síra a fosfor.
Příklad: C2H7N:
H3C ─ N ─ CH3 a H3C CH2 ─ NH2
│
H
dimethylamin ethylamin
(heterogenní) (homogenní)
Autor: Jennifer Fogaça
Vystudoval chemii
Chcete odkazovat na tento text ve školní nebo akademické práci? Dívej se:
FOGAÇA, Jennifer Rocha Vargas. „Řetězový izomerismus“; Brazilská škola. K dispozici v: https://brasilescola.uol.com.br/quimica/isomeria-cadeia.htm. Zpřístupněno 27. června 2021.
Chemie
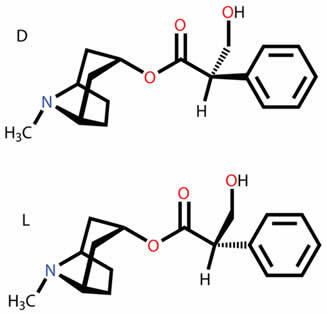
Zjistěte, o čem jsou různé typy rovinných a prostorových izomerů, jako je funkce, poloha, řetězec, tautomerismus, metamerismus, cis-trans geometrický a optický izomerismus.