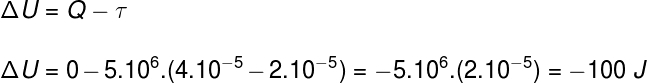طاقةداخلي هو مجموع الطاقات الحركية والإمكانات المتعلقة بحركة الذرات والجزيئات المكونة للجسم. الطاقة الداخلية أيضا تتناسب طرديا مع درجة الحرارة من الجسم. إنها كمية قياسية تقاس بالجول (SI) ويتم تحديدها كدالة لمتغيرات مثل الضغط (ف) ، أربعة حجمالخامس (الخامس) و درجة الحرارة الديناميكا الحرارية (T) لنظام ، في كلفن (ك).
كلما ارتفعت درجة حرارة الجسم ، زادت طاقته الداخلية ، وبالتالي ، زادت قدرته على القيام ببعض الأعمال. علاوة على ذلك ، فإن الطاقة الداخلية للغازات أحادية الذرة ، على سبيل المثال ، تُعطى حصريًا بمجموع الطاقة الحركية من كل ذرة من الغاز. عند التعامل مع الغازات الجزيئية ، مثل الغازات ثنائية الذرة ، يجب على المرء أن يأخذ في الاعتبار التفاعلات الجزيئية ، و هذا ، يتم تحديد الطاقة الداخلية من خلال مجموع الطاقة الحركية للجزيئات مع الطاقة الكامنة الموجودة بينهما أنهم.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
الطاقة الداخلية للغازات أحادية الذرة المثالية
نظرًا لعدم وجود تفاعل بين ذرات غاز أحادي الذرة المثالي ، فإن طاقته الداخلية تعتمد حصريًا على متغيرين: عدد المولات (n) ودرجة حرارة الغاز (T). يشاهد:
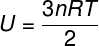
يو - الطاقة الداخلية
لا - عدد الشامات
ص - ثابت عالمي للغازات الكاملة
تي - درجة الحرارة
في المعادلة أعلاه ، ص معامله 0.082 صراف آلي. لتر / مول. كلفن أو 8.31 جول / مول. ك (SI). أيضًا ، يمكننا كتابة المعادلة أعلاه من حيث الكميات الأخرى ، مثل الضغط والحجم. لذلك ، نحن بحاجة إلى تذكر معادلة كلابيرون، تستخدم للغازات المثالية.
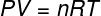
باستبدال المعادلة السابقة بالمعادلة السابقة ، سيكون لدينا التعبير التالي لحساب الطاقة الداخلية:
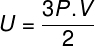
نظرةأيضا:ما هو الغاز المثالي؟
مع الأخذ في الاعتبار المعادلات أعلاه ، من الممكن تحديد العلاقة بين الطاقة الحركية لذرات غاز أحادي الذرة المثالي ودرجة حرارته. لهذا ، سنذكر أن الطاقة الحركية لهذا النوع من الغاز هي بحتةحركية. يشاهد:
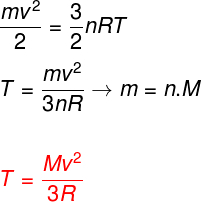
م - معكرونة
لا - رقم المول
م - الكتلة المولية
في كثير من الحالات ، من المثير للاهتمام معرفة كيفية حساب التغير في الطاقة الداخلية (ΔU) للغاز ، حيث تشير هذه الكمية إلى ما إذا كان الغاز وقد تلقت أو سلم طاقة. إذا كان التغير في الطاقة الداخلية للغاز موجبًا (ΔU> 0) ، فسيحصل الغاز على طاقة ؛ خلاف ذلك (ΔU <0) ، فإن الغاز سيكون قد تخلى عن جزء من طاقته.
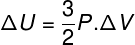
تغير الطاقة الداخلية من حيث تغير حجم الغاز.
الطاقة الداخلية للغازات ثنائية الذرة
بالنسبة للغازات ثنائية الذرة المثالية ، تُعطى الطاقة الداخلية بمعادلة مختلفة قليلاً.
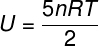
الطاقة الداخلية في التحولات والدورات الديناميكية الحرارية
وفقا ل القانون الأول للديناميكا الحرارية، يمكن أن تختلف الطاقة الداخلية للغاز المثالي بشكل معين التحولات الديناميكية الحرارية، اعتمادًا على كمية الحرارة المتبادلة بين المناطق المحيطة والنظام ، بالإضافة إلى العمل الذي يؤديه النظام أو عليه.
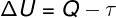
س - الحرارة
τ - الشغل
بعد ذلك ، لنلقِ نظرة على الشكل الذي يتخذه هذا القانون لبعض التحولات الديناميكية الحرارية.
نظرةأيضا:تاريخ الآلات الحرارية
→ الطاقة الداخلية: تحويل متساوي الحرارة
في تحول متساوي الحرارة، لا يوجد تغير في درجة الحرارة وبالتالي تظل الطاقة الداخلية ثابتة.
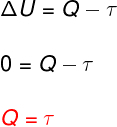
في هذه الحالة ، يتم تحويل كامل كمية الحرارة التي يتم تبادلها مع النظام إلى عمل والعكس صحيح.
→ الطاقة الداخلية: تحويل متساوي الحجم
في تحويل متساوي الحجم، لا يمكن تنفيذ العمل ، لأن النظام محصور في حاوية صلبة وغير قابلة للتوسيع. في هذه الحالة ، تختلف كمية الحرارة التي يتم تبادلها مع النظام بشكل مباشر عن طاقتها الداخلية.
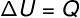
→ الطاقة الداخلية: تحويل متساوي الضغط
في هذا النوع من التحويل ، يخضع النظام لـ ضغط مستمرلذلك ، يمكن حساب العمل الذي قام به أو قام به بشكل تحليلي.
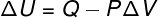
→ الطاقة الداخلية: تحول ثابت الحرارة
في ال التحولات الثابتة، لا يوجد تبادل حراري بين النظام ومحيطه ، وبالتالي ، فإن تباين الطاقة الداخلية يعتمد بشكل حصري على العمل الذي يؤديه النظام أو عليه.
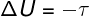
الطاقة الداخلية في العمليات الدورية
في كل عملية دورية ، تكون الحالة الديناميكية الحرارية للنظام ، ممثلة بمتغيرات الضغط والحجم ودرجة الحرارة (P ، V ، T) ، هي تحول ، ولكن ينتهي به الأمر بالعودة إلى الحالة الأصلية (P ، V ، T) ، وبالتالي فإن تباين الطاقة الداخلية في هذا النوع من العمليات يكون دائمًا فارغًا (ΔU = 0).
نظرةأيضا:التحولات الدورية
انظر إلى الرسم البياني أدناه ، والذي يُظهر ثلاثة تحولات ديناميكية حرارية مميزة بين الحالتين A و B.
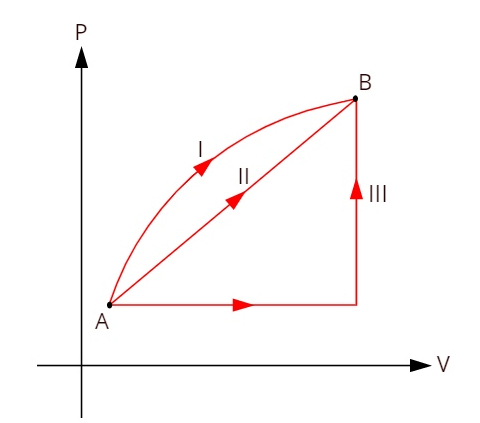
نظرًا لأن التحولات الثلاثة (I و II و III) تترك الحالة A وتنتقل إلى الحالة B ، يجب أن يكون تباين الطاقة الداخلية متساويًا بالنسبة لها جميعًا ، لذلك:
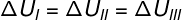
تمارين الطاقة الداخلية
1) تم العثور على مولين من غاز ثنائي الذرة مثالي ، مع كتلة مولارية تساوي 24 جم / مول ، عند درجة حرارة 500 كلفن داخل حاوية صلبة مغلقة بحجم يساوي 10-3 م³. تحديد:
أ) معامل الطاقة الداخلية لهذا الغاز بالجول.
ب) الضغط الذي يمارسه الغاز على جدران الحاوية.
القرار:
ال) نظرًا لأنه غاز مثالي وثنائي الذرة ، سنستخدم الصيغة أدناه لحساب طاقته الداخلية:
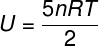
بأخذ البيانات التي تم إعلامنا بها في بيان التمرين ، سيكون لدينا الحساب التالي لحلها:
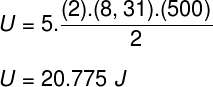
ب) يمكننا تحديد الضغط الذي يمارسه الغاز بمجرد معرفة حجم الحاوية الخاصة به: 10-3 م³. للقيام بذلك ، سوف نستخدم الصيغة التالية:
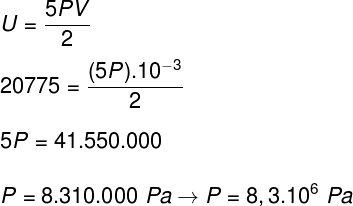
من جانبي رافائيل هيلربروك