النص تفاعلات الإضافة أظهر أن هذه الأنواع من التفاعلات العضوية تسمى بهذه الطريقة لأن مادة متفاعلة تضاف إلى الجزيء العضوي عن طريق كسر الروابط بين الكربون. في هذا النص ، تم عرض حالة الألكينات ، هنا سننظر بالفعل في كيفية حدوث ذلك مع الألكينات ، أو أي مع تلك الهيدروكربونات (التي تتكون فقط من ذرات الكربون والهيدروجين) التي لها رابطة ثلاثي.
النقطة الضعيفة للألكينات هي بالضبط الرابطة الثلاثية ، حيث يمكن كسر الروابط من نوع pi () (إضافة جزئية أو مرتين (إضافة كلية) وتؤدي ، على التوالي ، إلى مركبات جديدة ذات روابط مزدوجة (ألكينات) أو روابط مفردة (الألكانات).
لنلقِ نظرة على حالات تفاعلات الإضافة في الألكينات:
1. إضافة الهيدروجين أو الهدرجة:
في هذه الحالة ، جزيء H2 يضاف إلى الألكين باستخدام محفز ، والذي يكون عادة عبارة عن مسحوق نيكل (Ni) ، أو بلاتين (Pt) أو بلاديوم (Pd). بسبب الحاجة إلى استخدام محفز ، يسمى هذا التفاعل أيضًا الهدرجة الحفزية ويحدث على مراحل: في المرحلة الأولى تحصل على ألكين ، وفي المرحلة الثانية ، وهي أبطأ ، تحصل على ألكان.
إذا كان المحفز المستخدم قوياً ، مثل النيكل والبلاتين ، فإن التفاعل ينتج الألكان مباشرة. خليط البلاديوم مع BaSO
4 إنه محفز ضعيف وينتج الألكين. من الممكن أيضًا استخدام مثبط محفز جزئي للوصول إلى الألكين فقط. يحدث هذا التفاعل أيضًا تحت ضغوط ودرجات حرارة عالية.بعد ذلك ، لدينا إضافة الهيدروجين إلى الإيثان ، وإنتاج الإيثيلين ثم الإيثان:

2. إضافة الهالوجينات أو الهالوجين:
يتم كسر رابطة pi الخاصة بالكاين ويتم إضافة ذرتين هالوجين إلى الجزيء (عناصر من عائلة 17A من الجدول الدوري ، وأكثرها استخدامًا هي: Cl2 و Br2) ، وتشكيل ثنائي الهاليد المجاور ، مما يعني أن ذرتين من الهالوجين مرتبطة بذرات كربون مجاورة. يمكن أن يستمر التفاعل ، مما يؤدي إلى كسر رابطة pi الأخرى وإضافة ذرتين هالوجين أخريين إلى الجزيء.
في المثال أدناه ، لدينا هذا النوع من الإضافة إلى الرشوة:
ClCl ClCl
││ ││
ح C ≡ C CH3 + Cl2 → ح ج ═ C CH3 + Cl2 → ح ج ─ C CH3
││
ClCl
ALCINO DI-HALETTE TETRAHALETTE
3. إضافة هاليدات الهيدروجين (هالوجينهيدريد أو هيدروهلوجينيشن):
هنا ، يضاف هاليد الهيدروجين إلى الألكين ، ويمكن أيضًا إجراء الإضافة الجزئية والكاملة. أحد الجوانب المهمة لهذا النوع من التفاعل هو أنه يتبع حكم ماركوفنيكوف، أي أن الهيدروجين يرتبط بالكربون المهدرج أكثر (مع المزيد من ذرات الهيدروجين المرفقة) والهالوجين يرتبط بالكربون الأقل هدرجة.
في عملية الهالوجين الكلي ، يتم تكوين ثنائي الهاليد الجيمي ، أي مركب له ذرتان هالوجين متصلتان بنفس الكربون.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
يشاهد:
حBr Hر
││ ││
ح C ≡ C CH3 + HBr → ح ج ═ C CH3 + HBr → ح ج ─ C CH3
││
حر
ALCINO HALIDE GEMIC DI-HALOGIDE
أحد الأمثلة المهمة على هذا النوع من التفاعل هو ذلك الذي يحدث عند إضافة كلوريد الهيدروجين إلى ethyne ، مكونًا ال كلورو إيثين أو أحادي كلوريد الفينيل ، وهو المونومر الذي يشكل بوليمر البولي فينيل كلوريد ، المعروف بالاختصار PVC.
حClHCl
││ ││
ح C ≡ ج ─ ح + حمض الهيدروكلوريك → ح ج ═ ج ─ ح + حمض الهيدروكلوريك → ح ج ─ ج ─ ح
││
حCl
إيثينو كلوروتين 1،1-ثنائي كلورو إيثان
(مونومر PVC)
مادة PVC هي مادة تستخدم على نطاق واسع في الصناعة لتصنيع المنتجات المختلفة ، مثل الصنادل ، وزجاجات الأدوية ، والأجهزة الطبية ، والسراويل البلاستيكية للأطفال ، والحقائب ، طلاء الأسلاك ولعب الأطفال وتنجيد الأثاث وتنجيد السيارات ومعاطف المطر والأحذية البلاستيكية وسجلات الفينيل والأرضيات وأفلام التغليف والأنابيب المستخدمة في أنابيب المياه والصرف الصحي إلخ.
4. إضافة الماء (الترطيب):
في هذا التفاعل ، يتفاعل الماء مع الألكين ، مكونًا في البداية إنولًا ، والذي يخضع لإعادة ترتيب جزيئي ويتحول إلى ألدهيد (في حالة الألكينات الأصغر من الأسيتيلين). يظل الإينول والألدهيد في توازن ديناميكي مع غلبة الألدهيد. هذه حالة التماثل الديناميكي الديناميكي أو Tautomery.
مثال:

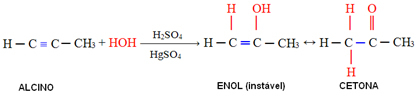
في حالة الألكينات الأكبر من الأسيتيلين ، يتم اتباع قاعدة ماركوفنيكوف ويؤدي إينول إلى تكوين الكيتون:
بقلم جينيفر فوغاسا
تخرج في الكيمياء



