تفاعلات الكبريتات في الألكانات هم انهم تفاعلات الإحلال العضوي، بهدف الإنتاج أحماض سلفونيك (المركبات العضوية التي تحتوي على مجموعة SO3H مرتبط بذرة كربون أو بسلسلة كربون) والماء (H2س).
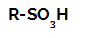
الصيغة التركيبية لحمض السلفونيك
لإجراء تفاعل sulfonation على الألكانات، يجب أن نخلط ألكان (مركب يتكون من سلسلة كربون مشبعة بذرات كربون وهيدروجين فقط) و حامض الكبريتيك (ح2فقط4) مركزة ، وتعرض للتسخين (∆).
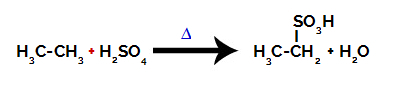
معادلة كيميائية تمثل سلفونة ألكان ثنائي الكربون
مبادئ تفاعل الكبريتات في الألكانات
مثل تفاعل كبريتات الألكان إنه تفاعل استبدال ، لدينا فيه تبادل بين المكونات الأصغر كهرسلبية من المواد المتفاعلة ، أي بين الألكان وحمض الكبريتيك. يحتوي الألكان على الهيدروجين وحمض الكبريتيك ومجموعة السلفونيك.
أدناه ، لدينا خطوة بخطوة آلية تفاعل السلفنة في الألكانات. كمثال ، سوف نستخدم أبسط ألكان ، الميثان (CH4):
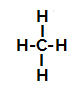
الصيغة الهيكلية للميثان
الخطوة الأولى: اضطراب الرابطة بين الهيدروكسيل (OH) والكبريت (S) في حامض الكبريتيك.
تتميز كل مجموعة هيدروكسيل موجودة في حامض الكبريتيك بأنها أكثر كهرسلبية. مع التسخين أثناء التفاعل ، يكون الاتجاه هو كسر الرابطة بين مجموعة الهيدروكسيل والكبريت:
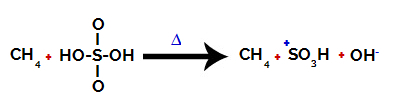
تمزق الرابطة بين الكبريت والهيدروكسيل
ومع ذلك ، فإن كسر رابطة جميع الهيدروكسيل لا يحدث بسبب إعادة الترتيب الإلكتروني في الهيكل. ثم يتم الحصول على أنيون هيدروكسيد (OH).-) وكاتيون سلفونيك.
الخطوة الثانية: تهاجم مجموعة الهيدروكسيل جزيء الألكان.
ثم مجموعة الهيدروكسي (OH-) يقوم بهجوم على الألكان ، مما يتسبب في كسر الرابطة بين الكربون والهيدروجين (وهو أكثر هشاشة بسبب الاختلاف في الكهربية بينهما).
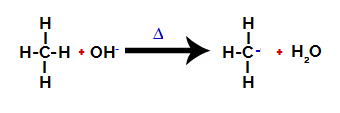
كسر الرابطة بين الكربون والهيدروجين في الألكان
ملحوظة: دائمًا ما يحدث اضطراب الرابطة بين الكربون والهيدروجين في كثير من الأحيان على الكربون ذي الكثافة الإلكترونية المنخفضة أو الشحنة الإلكترونية. كلما قل عدد الهيدروجين ، أو كلما زادت المجموعات المرتبطة به ، قلت كثافة الإلكترون. اذا لدينا:
الكربون الثلاثي
بعد كسر الرابطة ، يصبح الألكان كربون ناقص الإلكترون (carbocation). مجموعة الهيدروكسيد (OH)-) يتفاعل مع الهيدروجين المنطلق ويشكل جزيء ماء.
الخطوة الثالثة: هجوم الراديكالية المشكلة على مجموعة السلفونيك.
أخيرًا ، يتم مهاجمة مجموعة السلفونيك من قبل بقية الألكان ، مكونة حمض السلفونيك.
لا تتوقف الان... هناك المزيد بعد الإعلان ؛)
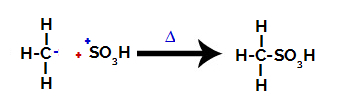
الهياكل التي تتفاعل وتشكل حمض السلفونيك
أمثلة على المعادلات التي تمثل تفاعلات السلفنة في الألكانات
المثال الأول: كبريتات البروبان.
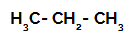
الصيغة الهيكلية للبروبان
يحتوي البروبان على كربونين أساسيين وكربون ثانوي ، ولهما شحنة مختلفة لأنهما مرتبطان بكميات مختلفة من الهيدروجين. نظرًا لأن الكربون أكثر كهرسلبيًا من الهيدروجين ، فإن هذه الكربونات لها كثافة إلكترون مختلفة.
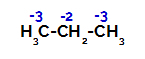
توزيع الشحنات على كل ذرة كربون من البروبان
في الكربون الأولي ، تكون الشحنة -3 (لأنها مرتبطة بثلاثة هيدروجين) ، وفي الكربون الثانوي ، تكون الشحنة -2 (لأنها مرتبطة بمركزي هيدروجين). وبالتالي ، سيكون هناك انقطاع في الرابطة بين الكربون والهيدروجين ، وأحيانًا عند الكربون 1 (لجزيء واحد) ، وأحيانًا عند الكربون 2 (لجزيء آخر).
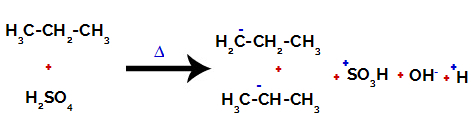
كسر الرابطة بين الكربون والهيدروجين على ذرات الكربون المختلفة
بعد الكسر بين الروابط ، سواء في حامض الكبريتيك والألكان ، هناك تكوين المنتجات مع استبدال الهيدروجين على الكربون 1 بمجموعة سلفونيك ، ويحدث الشيء نفسه على الكربون 2.
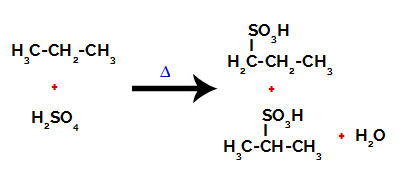
المنتجات المتكونة من سلفونة البروبان
المثال الثاني: كبريتات 2-ميثيل-بيوتان.

الصيغة التركيبية 2-ميثيل البيوتان
2-ميثيل البيوتان يحتوي على ثلاثة كربون أولية ، كربون ثانوي وكربون ثالث ، والتي لها شحنات مختلفة ، وبالتالي ، كثافات إلكترونية مختلفة ، كما يتضح من الهيكل التالي:
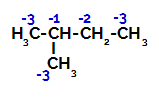
توزيع الشحنات الإلكترونية في 2-ميثيل بيوتان
لذلك يوجد في 2-ميثيل-بيوتان عدة احتمالات لكسر الرابطة بين الكربون والهيدروجين ، التي يمكن أن تحدث في الكربون 1 (لجزيء) ، أو الكربون 2 (لجزيء آخر) ، أو الكربون 3 أو الكربون 4. ومع ذلك ، من الجدير بالذكر أن الاضطراب في الكربون رقم 2 أكثر شيوعًا.
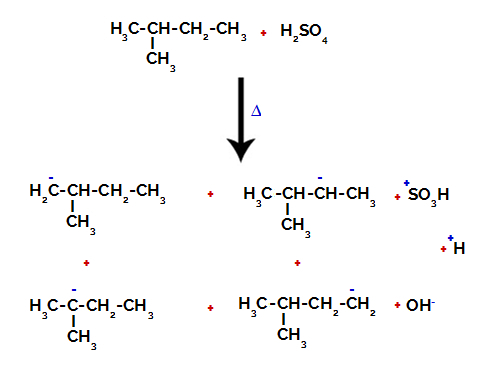
كسر الرابطة بين الكربون والهيدروجين على ذرات الكربون المختلفة
بعد الفواصل بين الروابط ، سواء في حمض الكبريتيك أو في الألكان ، يكون تكوين المنتجات مع استبدال الهيدروجين على الكربون 1 بمجموعة سلفونيك ، ويحدث نفس الشيء في الكربون 2.

المنتجات المتكونة من سلفنة 2-ميثيل البيوتان
بي ديوغو لوبيز دياس
هل ترغب في الإشارة إلى هذا النص في مدرسة أو عمل أكاديمي؟ نظرة:
DAYS ، ديوغو لوبيز. "تفاعلات الكبريتات في الألكانات" ؛ مدرسة البرازيل. متوفر في: https://brasilescola.uol.com.br/quimica/reacoes-sulfonacao-alcanos.htm. تم الوصول إليه في 28 يونيو 2021.