ا حمض الفورميك حصل على اسمه لأن الحصول عليه الأول كان من خلال تقطير النمل الأحمر (من اللاتينية فورميكا = النمل) ، والتي تحقن هذا الحمض الكربوكسيل من خلال لدغتها ، مما يسبب ألمًا شديدًا وتورم وحكة.
ومع ذلك ، فإن تسميته الرسمية هي حمض الميثانيك ، الذي يتم تمثيل صيغته الهيكلية أدناه:

بالإضافة إلى النمل ، يوجد حمض الميثانويك أيضًا في النحل والقراص وأشجار الصنوبر وبعض الفواكه.
في درجة حرارة الغرفة يكون عديم اللون ، سائل ، كاوي ، ذو رائحة قوية ومزعج. يستخدم هذا الحمض كمادة ، في إنتاج أول أكسيد الكربون ، في علاج الروماتيزم ، في إنتاج حمض الأكساليك ، كمبيد للجراثيم ، كمطهر ، وفي إنتاج منتجات أخرى عضوي.
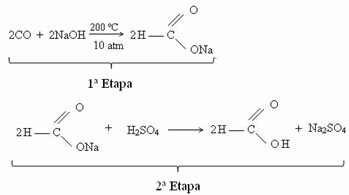
حاليًا ، يتم الحصول على حمض الفورميك من خلال التفاعل بين أول أكسيد الكربون والصودا الكاوية. رد الفعل هذا هو تقنية مشابهة لتلك التي تم تطويرها في عام 1855 من قبل الكيميائي الفرنسي مارسيلين بيرثيلوت (1827-1907). بعد ذلك ، لدينا هذا التفاعل ، حيث يتم الحصول على ميثانوات الصوديوم لأول مرة ، والذي ينتج حمض الميثانيك كأحد المنتجات بعد التفاعل مع حمض الكبريتيك:
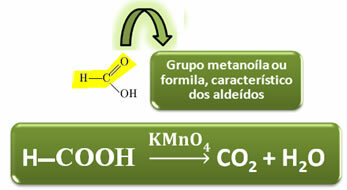
على عكس الأحماض الكربوكسيلية الأخرى ، يحتوي حمض الفورميك على مجموعة وظيفية من الألدهيدات ، مما يمنحه خاصية العمل كمخفض. يقلل من تفاعلات Fehling و Tollens ، التي تتأكسد لثاني أكسيد الكربون والماء.
بقلم جينيفر فوغاسا
تخرج في الكيمياء


