يتمثل عمل المحفز في الأساس في تسريع تطوير تفاعل معين. هذا ممكن لأن يغير المحفز الآلية التي يستمر بها التفاعل ، مما يؤدي إلى "مسار بديل" يتطلب طاقة تنشيط أقل لبدء التفاعل والوصول إلى المركب المنشط.
هناك عدة أنواع من الحفز الكيميائي ، أحدها هو تحفيز غير متجانس، والتي يمكن تعريفها على أنها هو ما يحدث عندما يكون للنظام أكثر من مرحلة ، أي أن المواد المتفاعلة والمنتجات في حالة فيزيائية مختلفة عن الحالة الفيزيائية للمحفز.
مثال يمكن أن نذكره هو مرحلة وسيطة من تكوين حامض الكبريتيك (H2فقط4 (عبد القدير)). تتكون هذه الخطوة من تكوين ثالث أكسيد الكبريت (SO3 (ز)) من خلال تفاعل احتراق ثاني أكسيد الكبريت (SO2 (ز)):
2 SO2 (ز) + س2 (ز) → 2 نظام تشغيل3 (ز)
مع استمرار هذا التفاعل ببطء شديد ، يتم استخدام محفز لتسريع هذا التفاعل. المحفز الذي يمكن استخدامه في هذه الحالة هو خامس أكسيد ديفاناديوم (V.2ا5 (صغير)) ، وهو صلب. نظرًا لأن المواد المتفاعلة ومنتج التفاعل غازية ، سيكون لدينا نظام غير متجانس.
ولكن كيف يمكن أن يسرع خامس أكسيد الديواناديوم رد الفعل؟
ما يحدث هو أن جزيئات كاشف الأكسجين ممتصة ، أي يتم الاحتفاظ بها على سطح خامس أكسيد ديفاناديوم. يؤدي هذا إلى إضعاف روابط جزيئات هذا الغاز بمرور الوقت ، مما يسهل تكوين المركب يتم تنشيطه ، وبالتالي يقلل من طاقة تنشيط التفاعل ، مما يزيد من معدل تطوره ، أي هو ● السرعة.
انظر كيف يحدث هذا في الرسم البياني أدناه:
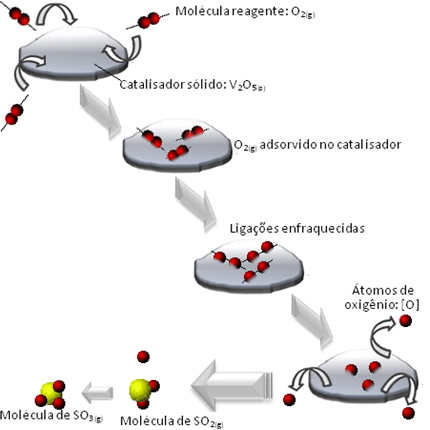
أمثلة أخرى من الحفز غير المتجانسة موضحة أدناه. لاحظ أنه في كلتا الحالتين تكون المواد المتفاعلة والمنتجات في الحالة الغازية أو المائية أو السائلة ، بينما تكون المحفزات في الحالة الصلبة:
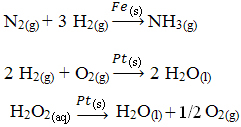
مثال على التحفيز غير المتجانس الذي يحدث في حياتنا اليومية هو المحولات محفز السيارة، المعروف باسم المحفزات. يتم تغليف هذه الأجهزة المضادة للتلوث بمواد تعمل كمحفزات عادة ما تكون سبيكة من البلاديوم والروديوم (لمحركات البنزين) والبلاديوم والموليبدينوم (لمحركات البنزين). كحول).
داخل هذا المحفز ، تحدث تفاعلات كيميائية يتم فيها تحويل الغازات الناتجة عن الاحتراق غير الكامل ، والتي تكون أكثر ضررًا للإنسان ، إلى غازات غير سامة. المواد المتفاعلة والمنتجات عبارة عن غازات ، بينما المحفزات عبارة عن مواد صلبة.
لفهم المزيد حول نظام تشغيل هذا الجهاز ، اقرأ النص: "المحول الحفاز”.
بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/catalise-heterogenea.htm

