يمكن إجراء التسمية الرسمية للإيثرات ، وفقًا لـ IUPAC ، بطريقتين. انظر كل واحد:
الطريقة الأولى:

أمثلة:
CH3 — ا — CH2 — CH3→ التقىأوكسيوآخروناا
CH3 — CH2 — ا — CH2 —CH3→ وآخرونأوكسيوآخروناا
CH3 — CH2 — ا — CH2— CH2 —CH3→وآخرونأوكسيدعماا
CH3 — ا — CH2— تشوش —CH3→ التقىأوكسيلكنenا
CH3 — CH2 — CH2 — ا — CH2— CH2 — CH2 — CH2 — CH3→دعمأوكسيمكبوتاا
إذا كانوا من إثيرات سلاسل مغلقة ، ستكون التسمية مختلفة:

أمثلة:
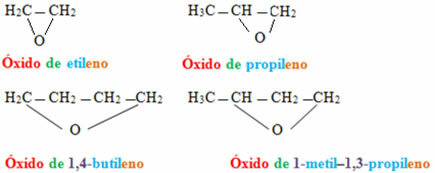
الطريقة الثانية:
تعتبر المجموعتان المرتبطتان بالأكسجين بدائل ، ويشار إليها بترتيب التعقيد مع اللاحقة ichأي أنه يتبع القاعدة التالية:
الأثير + المجموعة الأولى + المجموعة الثانية + ich
يجب أن تظهر هذه المجموعات و
أمثلة:
CH3— ا —CH2 —CH3→ الأثير إيثيلich و الميثيلich
CH3 —CH2—ا —CH2 —CH3→الأثيرثنائي إيثيلich
CH3 —CH2—ا —CH2—CH2 —CH3→الأثيرإيثيلich و بروبيلich
CH3 —CH2 —CH2—ا —CH2—CH2 —CH2 —CH2 —CH3→الأثيربروبيلich و بنتيلich
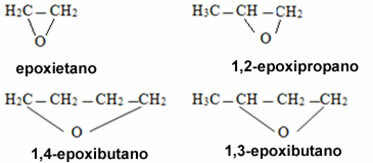
في حالة المركبات الحلقية تسمى الإيبوكسيدات:
بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/nomenclatura-dos-Eteres.htm
