أنت أحماض سلفونيك هي فئة من المركبات العضوية تتميز بالمجموعة الوظيفية أدناه:
R SO3ح
المجموعة الوظيفية (حمض السلفونيك)
يرمز الحرف "R" إلى أي جذري مشتق من الهيدروكربون. وبالتالي ، يمكن الحصول على أحماض السلفونيك من خلال تفاعل بين الهيدروكربون وحمض الكبريتيك ، في والتي يتم استبدال الهيدروجين الموجود في الهيدروكربون بحمض السلفونيك وتوليد الماء أيضًا ثانوية:
R─ح + ح─ هكذا3ح → R─ SO3ح + ح2ا
حمض الكبريتيك الهيدروكربوني ماء حامض السلفونيك
هذا الاعتبار للمجموعة ─ هكذا3ح كبديل للهيدروجين في الهيدروكربون يؤدي إلى التسمية المقترحة لهذه المركبات ، والتي يتم توفيرها من خلال القواعد التالية:

إذن لدينا الأمثلة:
ح3ج6 ─ 5CH2 ─ 4CH 3CH 2CH2─ 1CH3 : 4-ميثيل هكسان -3 حمض سلفونيك
│ │
CH3 فقط3ح
CH3 وبالتالي3H: حمض الميثان سلفونيك
CH3 ─ CH2وبالتالي3H: حمض إيثان سلفونيك
تشتهر أحماض السلفونيك بتطبيقها في الحصول على النبيذ الفوار الموجود في الشامبو والمنظفات ومعاجين الأسنان. تعمل هذه الأملاح كمواد خافضة للتوتر السطحي ، أي أنها تعمل عن طريق تقليل التوتر السطحي. الاسم العام لهذه الفئة من المركبات هو "السطحي". على الأسنان ، على سبيل المثال ، هذا هو مهم لأنه يسمح بالاختراق في الشقوق ويساعد على إزالة الحطام من سطح المينا. أكثر أنواع النبيذ الفوار شيوعًا المستخدمة في معجون الأسنان هو كبريتات لوريل الصوديوم (H.
3ج [CH2]10CH2OSO3في).تقلل المنظفات الاصطناعية المستخدمة كبدائل للصابون التوتر السطحي للماء ثم تسمح باستحلاب الزيوت والدهون. في البرازيل ، تحتوي المنظفات التركيبية الأنيونية عادةً على سلسلة مستقيمة من سلفونات ألكيل بنزين الصوديوم:
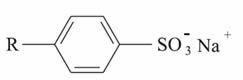
ومن الأنواع الأخرى المستخدمة على نطاق واسع ، لوريل سلفونات الصوديوم ، وهو ملح يتم الحصول عليه من خلال التفاعل الموصوف أدناه ، بين حمض السلفونيك وهيدروكسيد الصوديوم:
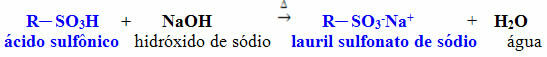
مثال آخر على الحصول على مركب بخصائص المنظف هو دوديكانس سلفونات الصوديوم ، والذي يتم الحصول عليه من خلال التفاعل أدناه ، من دوديكان -1- ol:
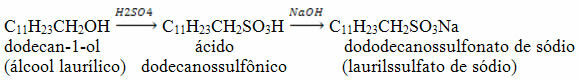
بقلم جينيفر فوغاسا
تخرج في الكيمياء
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/quimica/acidos-sulfonicos.htm
