ملح غيرعضوي تتشكل من خلال الارتباط الأيوني لكاتيون واحد على الأقل (يتكون من أي معدن أو بواسطة الأمونيوم) وأنيون (بسيط أو مركب).
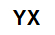
الصيغة الجزيئية العامة للملح
عند إضافتها إلى الماء ، تنفصل الأملاح ، وتطلق على الأقل كاتيون واحد غير الهيدرونيوم (H+) وأنيون غير الهيدروكسيد (OH-).
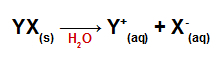
معادلة تفكك أي ملح
تصنيف الأملاح
يمكن أن تحتوي الأملاح بشكل عام على التصنيفات التالية:
ملح بسيط: ملح يتكون من كاتيون واحد وأنيون واحد. أمثلة: NaCl ، CaSO4، KCN ، NH4كو3 إلخ.
ملح مهدرج: له اثنين من الكاتيونات (يجب أن يكون أحدهما هيدرونيوم) وأنيون. أمثلة: NaHCO3، CaHBO3 إلخ.
ملح الهيدروكسيل: لها كاتيون وأنيونان (يجب أن يكون أحدهما هيدروكسيد). أمثلة: MgOHCl ، Al (OH)2ClO3 إلخ.
ملح رطب: يعرض جزيئات الماء المرتبطة بهيكله البلوري. أمثلة: CaCl2.2H2يا ، CuSO46 ح2الخ.
ملح مزدوج: له اثنين من الكاتيونات (كلها مختلفة عن الهيدرونيوم) وأنيون واحد أو كاتيون واحد وأنيونان (كلها مختلفة عن الهيدروكسيد). أمثلة: النوع4CN ، AgFeBO3 إلخ.
الشب: هو الملح الذي يتكون من كبريتين مع كاتيونات أكاسيد النيتروجين تساوي +1 و +3 ، بالإضافة إلى 24 جزيء من الماء. أمثلة: Ag2فقط4.Al2(فقط4)3.24H2على2فقط4.Sb2(فقط4)3.24H2ا
قاعدة تسمية الملح
اسم أنيون + دي + اسم الكاتيون
→ ك3غبار4
يحتوي الملح على أنيون الفوسفات (PO4-3) وكاتيون البوتاسيوم (K.+1) ، ومن هنا جاء اسمها فوسفات البوتاسيوم.
→ حالة3
الملح يحتوي على أنيون الكبريتيت (SO3-2) وكاتيون الكالسيوم (Ca+2) ، ومن هنا اسمها هو كبريتات الكالسيوم.
ملاحظة: إذا لم يكن الكاتيون من الفضة أو الزنك أو عنصرًا ينتمي إلى عائلات IA و IIA و IIIA ، فيجب أن نشير إلى أكاسيد النيتروجين برقم روماني أمام اسم الكاتيون.
→ نحاس2فقط4
يحتوي الملح على أنيون الكبريتات (SO4-2) وكاتيون الكالسيوم (Cu+1) ، ومن هنا جاء اسمها كبريتات النحاس 1.
ملح مهدرج: بالنسبة لهذا الملح ، قبل اسم الأنيون ، يجب أن نكتب البادئة التي تشير إلى كمية الهيدروجين في الصيغة. يجب أن تكون هذه البادئة منفصلة عن الكلمة هيدروجين بشرطة.
→ ناهكو3
يحتوي الملح على هيدروجين وأنيون كربونات وكاتيون صوديوم ، لذا فإن اسمه هو كربونات أحادي الهيدروجين الصوديوم.
ملح الهيدروكسيل: لهذا الملح ، قبل اسم الأنيون ، يجب أن نكتب البادئة التي تشير إلى كمية الهيدروكسيل في الصيغة. يجب أن تكون هذه البادئة منفصلة عن الكلمة هيدروكسي بشرطة.
→ آل (أوه)2ClO3
يحتوي الملح على نوعين من الهيدروكسيل ، أنيون الكلورات وكاتيون الألومنيوم ، لذا فإن اسمه هو الألومنيوم ثنائي هيدروكسي كلورات.
ملح رطب: لهذا الملح ، بعد اسم الكاتيون ، يجب أن نكتب البادئة التي تشير إلى كمية جزيئات الماء في الصيغة. يجب أن تكون هذه البادئة منفصلة عن الكلمة رطب بشرطة.
→ كاكل2.2H2ا
يحتوي الملح على جزيئين من الماء ، أنيون الكلوريد وكاتيون الكالسيوم ، لذلك اسمه هو ثنائي هيدرات كلوريد الكالسيوم.
ملح مزدوج مع كاتيونات: بالنسبة لهذا الملح ، يجب أن نكتب الكلمة المزدوجة بين قوسين بعد اسم الأنيون ثم اسم الكاتيون الأكثر حساسية للكهرباء واسم الكاتيون الآخر.
→ AgFeBO3
يحتوي هذا الملح على الفضة (كاتيون أكثر حساسية للكهرباء) وكاتيون الحديد II ، بالإضافة إلى أنيون البورات. اسمها بورات (مزدوج) من الفضة والحديد الثاني.
-
ملح مزدوج مع أنيونين:
اسم معظم الأنيون الكهربية + الواصلة + اسم الأنيون الكهربي + الاسم الموجب له
→ يكتب4CN
يحتوي هذا الملح على كاتيون التيتانيوم الرابع ، بالإضافة إلى الفوسفات (أنيون أكثر كهرسلبية) وأنيون السيانيد. اسمها هو فوسفات التيتانيوم السيانيد الرابع.
ملح الشب: لهذا الملح ، نتجاهل القاعدة العامة. ما عليك سوى كتابة المصطلح الشب متبوعًا باسم كاتيون الشحنة +3 واسم كاتيون الشحنة +1 ، على التوالي ، مفصولة بالتزامن e.
→ في2فقط4.Sb2(فقط4)3.24H2ا
يحتوي ملح الشب على كاتيون الأنتيمون +3 وكاتيون الصوديوم +1 ، لذلك اسمه هو الأنتيمون III الشب والصوديوم.
الخصائص الفيزيائية للأملاح
تكون صلبة في درجة حرارة الغرفة.
لديهم نقاط انصهار وغليان عالية ؛
تتشكل من روابط أيونية.
يجرون تيارًا كهربائيًا في الحالة السائلة (بعد الخضوع للاندماج) أو عند إذابته في الماء ؛
بشكل عام ، فهي قابلة للذوبان في الماء ، ولكن هناك أملاح تعتبر غير قابلة للذوبان عمليا.
الخواص الكيميائية للأملاح
الأملاح هي مركبات لها القدرة على التفاعل كيميائيًا (بشرط ألا تحتوي على نفس الكاتيون أو نفس الأنيون مثل مادة أخرى) مع عدة مجموعات من المواد ، وهي:
في تفاعل مزدوج مع حمض: يشكلون ملحًا جديدًا وحمضًا جديدًا.
في تفاعل مزدوج مع قاعدة: يشكلون ملحًا جديدًا وقاعدة جديدة.
في تفاعل التبادل المزدوج مع ملح آخر: تشكيل اثنين من الأملاح الجديدة.
بعض الأملاح لديها القدرة على المعاناة تقسيم عند التعرض للحرارة ، تكون مادتين جديدتين أو أكثر. إذا قمنا بتسخين بيكربونات الصوديوم (NaHCO3) ، على سبيل المثال ، سوف يتحلل مكونًا كربونات الصوديوم (Na2كو3) ، ماء (H2O) وثاني أكسيد الكربون (CO2).
بي ديوغو لوبيز دياس
مصدر: مدرسة البرازيل - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-sao-sais-inorganicos.htm
